20.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 9g甲基(-CH3)所含有的电子数是10 NA个 | |
| B. | 22.4L乙烷中含有的共价键数为7NA个 | |
| C. | 常温下,14g乙烯和丙烯的混合物中总原子数为3NA个 | |
| D. | 4.2g C3H6中含有的碳碳双键数一定为0.1NA |
18.镁有三种同位素24Mg、25Mg、26Mg,氯有两种天然同位素35Cl、37Cl,那么氯化镁的相对分子质量的数值应有( )
| A. | 3种 | B. | 5种 | C. | 7种 | D. | 9种 |
16.制备新型高效水处理剂高铁酸钠(Na2FeO4)的主要反应为:2FeSO4+aNa2O2═2Na2FeO4+2Na2O+2Na2SO4+bX.下列说法中正确的是( )
| A. | 该反应中X物质为O2 | |
| B. | 反应物Na2O2只做氧化剂 | |
| C. | 该反应中发生氧化反应的过程只有FeSO4→Na2FeO4 | |
| D. | 每生成lmol Na2FeO4,反应过程中转移4 mol e- |
13.某元素的一种核素${\;}_{N}^{A}$X,它与2H原子组成HmX分子,在a g HmX中所含中子的物质的量是( )
| A. | $\frac{a}{A}$(A-N)mol | B. | $\frac{a}{A+2m}$ (A-N+m)mol | C. | $\frac{a}{A+2m}$(A-N)mol | D. | $\frac{a}{A+m}$(A-N+m)mol |
12.下列实验能达到实验目的是( )
| 序号 | 实验操作 | 实验目的 |
| A | A l、Mg分别与稀氢氧化钠溶液反应 | 比较铝、镁的金属性强弱 |
| B | 2mol/LNaOH溶液滴加到1mol/LCaCl2溶液中,产生白色沉淀 | 比较钠、钙的金属性强弱 |
| C | 用盐酸和碳酸钙反应制取的CO2直接通入Na2SiO3溶液中,溶液变浑浊 | 比较碳、硅的非金属性强弱 |
| D | Cl2、Br2分别与H2反应 | 比较氯、溴的非金属性强弱 |
| A. | A | B. | B | C. | C | D. | D |
11.下列说法不正确的是( )
0 154542 154550 154556 154560 154566 154568 154572 154578 154580 154586 154592 154596 154598 154602 154608 154610 154616 154620 154622 154626 154628 154632 154634 154636 154637 154638 154640 154641 154642 154644 154646 154650 154652 154656 154658 154662 154668 154670 154676 154680 154682 154686 154692 154698 154700 154706 154710 154712 154718 154722 154728 154736 203614
| A. | 铅蓄电池在放电过程中,电池反应液的pH将变小 | |
| B. | 相同条件下,结合质子的能力:OH->ClO->CH3COO- | |
| C. | 一定条件下,使用催化剂能加快反应速率并提高反应物的平衡转化率,平衡常数保持不变 | |
| D. | 在氯化银悬浊液中加入NaBr溶液,沉淀由白色转变为淡黄色,说明Ksp(AgCl)>Ksp(AgBr) |
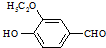 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.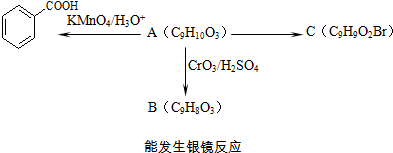
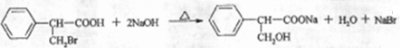
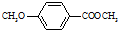 )是一种医药中间体.
)是一种医药中间体. )合成D.用反应流程图表示如下,请将后面一步的反应条件写在箭头下方,试剂或原料写在箭头上方,中间产物填在图中的方框内.
)合成D.用反应流程图表示如下,请将后面一步的反应条件写在箭头下方,试剂或原料写在箭头上方,中间产物填在图中的方框内.



