1.标况下将CO2气体缓缓地通入到含2mol KOH、1mol Ba(OH)2和2mol KAlO2的混合溶液中直至过量,生成沉淀的物质的量与所通CO2的体积关系如图所示.下列关于整个反应进程中的各种描述正确的是( )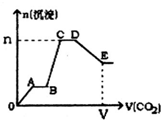

| A. | A~B段和C~D段发生的反应相同 | |
| B. | B~C段反应的离子方程式是 A1O2-+2H2O+CO2═Al(OH)3↓+HCO3- | |
| C. | V=134.4L,n=3mol | |
| D. | D点所得溶液中离子浓度关系为c(K+)>c(CO${\;}_{3}^{2-}$)>c(OH-)>c(HCO${\;}_{3}^{-}$)>c(H+) |
20.短周期元素X、Y、Z、W在周期表中的相对位置如下表所示,已知它们的最外层电子数之和为21,下列说法一定正确的是( )
| X | Y | Z | W |
| A. | X、Y、Z、W中至少有一种是金属元素 | |
| B. | 元素的最高化合价:W>Z>Y | |
| C. | 简单离子半径由大到小的顺序:W>Z>Y>X | |
| D. | 一定条件下,W的单质可以置换出Z的单质 |
19.2015年,我国科学家屠呦呦因发现青蒿素而荣获诺贝尔奖.由植物黄花蒿叶中提取的青蒿素还可合成用于抗氯喹恶性疟及凶险型疟疾的蒿甲醚,其合成路线如下:下列说法不正确的是( )
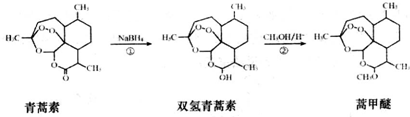

| A. | 青蒿素的分子式是C15H22O5,属于烃的衍生物 | |
| B. | 青蒿素难溶于水,而易溶于有机溶剂 | |
| C. | 反应②为取代反应,有H2O生成 | |
| D. | 青蒿素遇湿润的淀粉碘化钾试纸立刻显蓝色,是因为分子结构中含有酯基 |
18.下列各组离子,在指定的条件下一定能大量共存的是( )
| A. | NH4Fe(SO4)2的溶液中:H+、Mg2+、Br-、NO3- | |
| B. | 含有大量HCO3-的溶液:NH4+、Ca2+、AlO2-、I- | |
| C. | 浓度为3%的H2O2溶液:H+、Fe2+、C1-、SO42- | |
| D. | c(S2-)=0.1mo1.L-1的溶液中:Na+、NH4+、ClO-、SO42- |
17.民以食为天,食品安全越来越受到大家的关注.下列有关说法正确的是( )
| A. | 二氧化硫有毒,严禁将其添加到任何食品和饮料中 | |
| B. | 饮食“镉大米”会影响骨骼和肾脏,镉元素属于重金属元素 | |
| C. | 使用增塑剂--邻苯二甲酸酯可使聚氯乙烯由弹性塑胶变为硬塑胶 | |
| D. | 面粉生产中禁止添加的过氧化钙(CaO2)中阴阳离子的个数比为1:2 |
16.草酸钴用途广泛,可用于指示剂和催化剂的制备.一种利用水钴矿[主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、MgO、CaO等]制取CoC2O4的工艺流程如下:
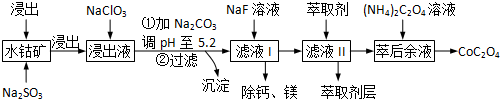
己知:,①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
(1)浸出过程中加入Na2SO3的目的是将Fe3+、Co3+还原.
(2)NaClO3可将Fe2+氧化为Fe3+离子.可用氯气通入到热的浓氢氧化钠溶液来制取NaClO3.实验需要制取10.65克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为6.72L(标准状况下).
(3)萃取剂对金属离子的萃取率与pH的关系如下图所示.使用萃取剂最适宜的pH是B(填选项序号).
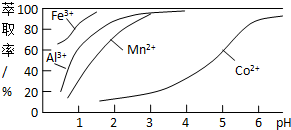
A.接近2.0 B.接近3.0 C.接近5.0
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知某温度下,Ksp(MgF2)=7.35×10-11,Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=0.7.
(5)为测定制得的无水草酸钴样品的纯度,现称取样品mg,先用适当试剂将其转化,得到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用c mol/L高锰酸钾溶液去滴定,当溶液由无色变为浅紫色(或紫红色),且半分钟内不变色时(填颜色变化),共用去高锰酸钾溶液VmL,计算草酸钴样品的纯度为36.75cv/m%.

己知:,①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(2)NaClO3可将Fe2+氧化为Fe3+离子.可用氯气通入到热的浓氢氧化钠溶液来制取NaClO3.实验需要制取10.65克NaClO3,需要的氯气由电解食盐水生成,若不考虑反应过程中的损失,则同时生成的氢气的体积为6.72L(标准状况下).
(3)萃取剂对金属离子的萃取率与pH的关系如下图所示.使用萃取剂最适宜的pH是B(填选项序号).

A.接近2.0 B.接近3.0 C.接近5.0
(4)“除钙、镁”是将溶液中Ca2+与Mg2+转化为MgF2、CaF2沉淀.已知某温度下,Ksp(MgF2)=7.35×10-11,Ksp(CaF2)=1.05×10-10.当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+)=0.7.
(5)为测定制得的无水草酸钴样品的纯度,现称取样品mg,先用适当试剂将其转化,得到纯净的草酸铵溶液,再用过量的稀硫酸酸化,用c mol/L高锰酸钾溶液去滴定,当溶液由无色变为浅紫色(或紫红色),且半分钟内不变色时(填颜色变化),共用去高锰酸钾溶液VmL,计算草酸钴样品的纯度为36.75cv/m%.
15.工业上有一种用CO2生产甲醇的方法:CO2(g)+3H2(g)?CH3OH(g)+H2O(g)+49kJ,现将6molCO2和8molH2充入20L的密闭容器中,测得H2的物质的量随时间变化如图所示,a、b、c、d括号内数据表示坐标.下列说法正确的是( )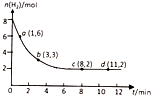
0 154521 154529 154535 154539 154545 154547 154551 154557 154559 154565 154571 154575 154577 154581 154587 154589 154595 154599 154601 154605 154607 154611 154613 154615 154616 154617 154619 154620 154621 154623 154625 154629 154631 154635 154637 154641 154647 154649 154655 154659 154661 154665 154671 154677 154679 154685 154689 154691 154697 154701 154707 154715 203614

| A. | 升高温度,平衡常数将变大 | B. | 0~1min,v(CO2)=0.1mol/(L•min) | ||
| C. | 达到平衡时,氢气的转化率为75% | D. | 到达平衡时,甲醇的体积分数为20% |
 ,F
,F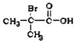 .
.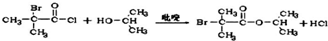 .
.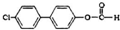 .
.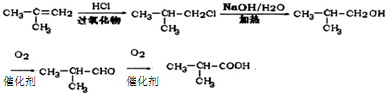 .
.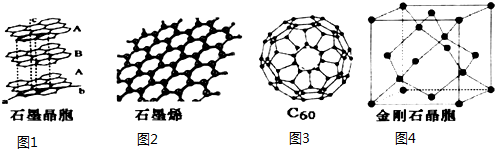

 +NaOH$→_{△}^{CuO}$R-H+Na2CO3
+NaOH$→_{△}^{CuO}$R-H+Na2CO3 .
.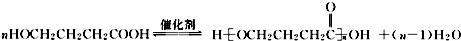 .
.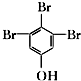 (写结构简式).
(写结构简式).