2.下列有关实验操作、现象和解释或结论都正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 向足量AgNO3溶液中先滴加少量NaCl溶液,后滴加少量KI溶液 | 先产生白色沉淀后又产生黄色沉淀 | AgI比AgCl更难溶 |
| B | 溴乙烷和烧碱的乙醇溶液共热 | 产生的气体可使酸性高锰酸钾溶液褪色 | 证明有乙烯生成 |
| C | 将高温水蒸气通过灼热的铁粉 | 铁粉变红 | 铁与水在高温下能发生反应 |
| D | Fe粉中加入过量的稀HNO3,充分反应后滴入几滴KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
1.有三种短周期元素,最外层电子数之和为17,质子数之和为31.如果这三种元素中有一种是氩元素,则关于另外两种元素的说法不正确的是( )
| A. | 两元素必在同一周期 | B. | 两元素可能在相邻两周期 | ||
| C. | 两元素不可能同为金属元素 | D. | 两元素不可能同主族 |
19.已知1molX2完全燃烧生成X2O放出热量a kJ.且氧气中1molO=O键完全断裂时吸收热量b kJ,X2O中1molX-O键形成时放出热量c kJ,X2中1molX-X键断裂时吸收热量为( )
| A. | 4c-b+2a kJ | B. | $\frac{4c-b-2a}{2}$ kJ | C. | 4c+b-2a kJ | D. | $\frac{4c+b-2a}{2}$ kJ |
18.已知五种短周期元素的原子半径及主要化合价如下表:
下列叙述正确的是( )
0 154308 154316 154322 154326 154332 154334 154338 154344 154346 154352 154358 154362 154364 154368 154374 154376 154382 154386 154388 154392 154394 154398 154400 154402 154403 154404 154406 154407 154408 154410 154412 154416 154418 154422 154424 154428 154434 154436 154442 154446 154448 154452 154458 154464 154466 154472 154476 154478 154484 154488 154494 154502 203614
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.102 | 0.089 | 0.074 |
| 主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
| A. | L与Q形成的化合物化学式为LQ | |
| B. | L、M的单质与稀盐酸反应剧烈程度:M>L | |
| C. | Q、T的氢化物在常温常压下均为无色气体 | |
| D. | M的最高价氧化物的水化物不具有两性 |
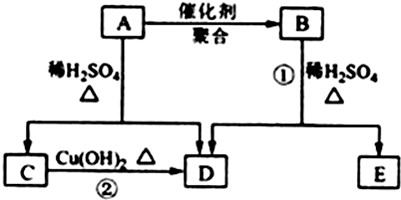
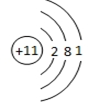 .
. 盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
盐酸、硫酸和硝酸是中学阶段常见的“三大酸”.现就硫酸、硝酸与金属铜反应的情况,回答下列问题: