题目内容
14.D3O+所含电子数为10.分析 阳离子的电子数=该元素的原子序数-所带电荷的数值,据此解题.
解答 解:阳离子的电子数=该元素的原子序数-所带电荷的数值=11-1=10,故答案为:10.
点评 本题考查原子结构、提取信息能力等,难度中等,根据阳离子的电子数=该元素的原子序数-所带电荷的数值是解题关键.

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目
4.下列有关说法错误的是( )
| A. | 微粒半径Na+<K+<Cl-<S2- | B. | 稳定性HI>HBr>HCl>HF | ||
| C. | 酸性H2SiO3<H3PO4<H2SO4<HClO4 | D. | 碱性KOH>Ca(OH)2>Mg(OH)2>Al(OH)3 |
19.已知1molX2完全燃烧生成X2O放出热量a kJ.且氧气中1molO=O键完全断裂时吸收热量b kJ,X2O中1molX-O键形成时放出热量c kJ,X2中1molX-X键断裂时吸收热量为( )
| A. | 4c-b+2a kJ | B. | $\frac{4c-b-2a}{2}$ kJ | C. | 4c+b-2a kJ | D. | $\frac{4c+b-2a}{2}$ kJ |
6.下列各组主族原子中,彼此化学性质一定相似的是( )
| A. | 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 | |
| B. | 原子核外M层上有5个电子的X原子与原子核外N层上有5个电子的Y原子 | |
| C. | 2p轨道上有一个未成对电子的X原子与3p轨道上有一个未成对电子的Y原子 | |
| D. | 最外层都只有一个电子的X、Y原子 |
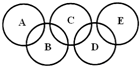 如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为
如图所示的五元环代表A、B、C、D、E五种化合物,圆圈交叉部分指两种化合物含有一种相同元素,五种化合物由五种短周期元素形成,每种化合物仅含两种元素,A是沼气的主要成分,B、E分子中所含电子数均为18,B不稳定,具有较强的氧化性,其稀溶液是医疗上广泛使用的消毒剂,E的分子结构模型为 ,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题:
,C可作为光导纤维的主要材料,D中所含两种元素的原子个数比为3:4,电子总数之比为3:2.根据以上信息回答下列问题: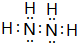 .
. X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X只有一种原子轨道,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.
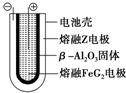
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X只有一种原子轨道,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子. Fe+2ZG
Fe+2ZG

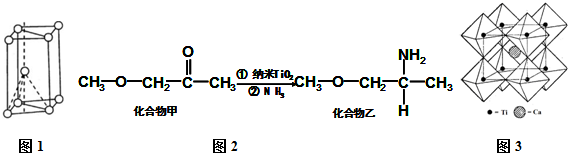
 ,其原子核外共有22种运动状态不相同的电子.金属钛晶胞如下图1所示,为六方最密堆积(填堆积方式).
,其原子核外共有22种运动状态不相同的电子.金属钛晶胞如下图1所示,为六方最密堆积(填堆积方式).