2.下列说法不正确的是( )
| A. | 现代化学元素分析测试中,可用元素分析仪确定物质中是否含有C、H、O、N、S、Cl、Br等元素,用红外光谱仪确定物质中是否存在某些有机原子团,用原子吸收光谱确定物质中含有哪些金属元素等 | |
| B. | 钠钾合金在常温下是液体,可用于快中子反应堆作剂;镁合金大量用于制造火箭、导弹和飞机的部件等 | |
| C. | 2015年浙江省多地遭遇雾霾天气,有报道称雾霾颗粒中汽车尾气占20%以上,一致汽车尾气中的主要污染物为NOx、CO、燃烧源超细颗粒(PM2.5)等有害物质,其中PM2.5(OM单位为百万分之一米)颗粒大小约等于胶体粒子 | |
| D. | 如图所示为四大基本反应及其关系,则反应4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O属于区域3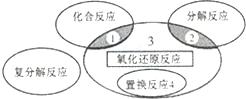 |
1.四种常见元素的性质或结构信息如表,根据信息回答有关问题.
(1)A元素与其同周期相邻两种元素原子的第一电离能由大到小的顺序为N>O>C(用元素符号表示);试解释原因同周期随原子序数增大,元素第一电离能呈增大趋势,氮元素2p能级为半满稳定状态,第一电离能高于同周期相邻元素的.
(2)B元素的低价氧化物分子中心原子的杂化方式为sp2杂化,B元素的最高价氧化物分子的VSEPR构型为平面三角形;B元素与D元素形成分子空间构型为直线形;
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2是分子晶体,SiO2是原子晶体;
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为先生成蓝色沉淀,后沉淀溶解,最后得到深蓝色溶液;后一现象的离子方程式为:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++4H2O+2OH-.
(5)C晶体的堆积方式如图所示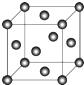 ,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{4×64}{{a}^{3}×{N}_{A}}$g•cm-3(要求写表达式,可以不简化).
,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{4×64}{{a}^{3}×{N}_{A}}$g•cm-3(要求写表达式,可以不简化).
| 元素 | A | B | C | D |
| 性质 或结 构信息 | 原子核外有两个电子层,最外层有3个未成对电子 | 原子的M层有1对成对的p电子 | 原子核外电子排布为:[Ar]3 d104sx,有+1、+2两种常见化合价 | 有两种常见氧化物,其中一种是冶炼金属工业的常用还原剂 |
(2)B元素的低价氧化物分子中心原子的杂化方式为sp2杂化,B元素的最高价氧化物分子的VSEPR构型为平面三角形;B元素与D元素形成分子空间构型为直线形;
(3)D元素最高价氧化物的熔点比同主族相邻元素最高价氧化物的熔点低(填“高”或“低”),其原因是CO2是分子晶体,SiO2是原子晶体;
(4)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,观察到的现象为先生成蓝色沉淀,后沉淀溶解,最后得到深蓝色溶液;后一现象的离子方程式为:Cu(OH)2+4NH3•H2O═[Cu(NH3)4]2++4H2O+2OH-.
(5)C晶体的堆积方式如图所示
 ,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{4×64}{{a}^{3}×{N}_{A}}$g•cm-3(要求写表达式,可以不简化).
,设晶胞边长为a cm,阿伏伽德罗常数用NA表示,则晶胞中C原子的配位数为12,C晶体的密度为$\frac{4×64}{{a}^{3}×{N}_{A}}$g•cm-3(要求写表达式,可以不简化).
20.已知室温下,0.1mol•L-1某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A. | HA电离出的c(H+)与水电离出的c(H+)之比为108 | |
| B. | 升高温度,溶液的pH减小 | |
| C. | 溶液的pH=4 | |
| D. | HA的电离平衡常数约为l×10-7 |
19.利用如图装置探究温度对氨气还原Fe203的影响(固定装置略).
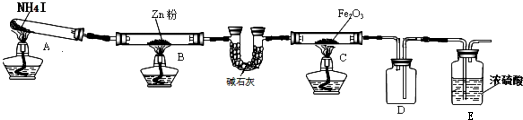
(1)实验时A中有大量紫红色的烟气,则NH4I的分解产物为NH3、H2、I2(HI)(至少填三种),碱石灰的作用是干燥及吸收酸性气体
(2)装置B中的反应化学方程式Zn+I2═ZnI2,D装置的作用是安全瓶,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置C加热,反应产物均为黑色粉末(纯净物),两组分别用各自的产物进行以下探究,完成下列填空:
(3)乙组得到的黑色粉末是Fe;
(4)步骤1甲组中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O;
(5)步骤3乙组中溶液变红的原因为Fe2+被氧化为Fe3+,Fe3+遇SCN-显红色,
(6)若装置C中反应后的固体是Fe203和Fe0组成的混合物.为确定其组成.取样品7.84克,在加热条件下通入氨气,完全反应后,停止加热,反应管中铁粉冷却后,称得质量为5.6克,则混合物中Fe203和Fe0的物质的量之比为2:1.

(1)实验时A中有大量紫红色的烟气,则NH4I的分解产物为NH3、H2、I2(HI)(至少填三种),碱石灰的作用是干燥及吸收酸性气体
(2)装置B中的反应化学方程式Zn+I2═ZnI2,D装置的作用是安全瓶,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置C加热,反应产物均为黑色粉末(纯净物),两组分别用各自的产物进行以下探究,完成下列填空:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无明显变化 |
| 3 | 向步骤2溶液中滴加新制氯水 | 红色先变深后褪去 | 先变红后也褪色 |
(4)步骤1甲组中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O;
(5)步骤3乙组中溶液变红的原因为Fe2+被氧化为Fe3+,Fe3+遇SCN-显红色,
(6)若装置C中反应后的固体是Fe203和Fe0组成的混合物.为确定其组成.取样品7.84克,在加热条件下通入氨气,完全反应后,停止加热,反应管中铁粉冷却后,称得质量为5.6克,则混合物中Fe203和Fe0的物质的量之比为2:1.
17.下列有关化学用语表示正确的是( )
| A. | CO 2分子比例模型: | B. | S 2-的结构示意图: | ||
| C. | 中子数为20的氯原子:${\;}_{17}^{20}$Cl | D. | HCN分子的结构式:H-C≡N |
16.居室装修用石材的放射性常用${\;}_{88}^{226}$Ra作为标准,发现Ra元素的居里夫人(Marie Curie)曾两度获得诺贝尔奖.下列叙述中正确的是( )
| A. | ${\;}_{88}^{226}$Ra原子核外有88个电子 | |
| B. | Ra元素位于元素周期表中第六周期ⅡA族 | |
| C. | RaCl2的熔点比CaCl2高 | |
| D. | Ra(OH)2是一种两性氢氧化物 |
15.下列说法中正确的是( )
0 154288 154296 154302 154306 154312 154314 154318 154324 154326 154332 154338 154342 154344 154348 154354 154356 154362 154366 154368 154372 154374 154378 154380 154382 154383 154384 154386 154387 154388 154390 154392 154396 154398 154402 154404 154408 154414 154416 154422 154426 154428 154432 154438 154444 154446 154452 154456 154458 154464 154468 154474 154482 203614
| A. | 配制240mL 0.1mol/LCuSO4溶液需称取胆矾6.3g | |
| B. | 金属氧化物一定是碱性氧化物 | |
| C. | 1L水中溶解58.5g NaCl,该溶液中NaCl的物质的量浓度为1 mol•L-1 | |
| D. | 胶体区别于其他分散系的本质特征是能够产生丁达尔效应 |
 .
. ,
,