题目内容
15.下列说法中正确的是( )| A. | 配制240mL 0.1mol/LCuSO4溶液需称取胆矾6.3g | |
| B. | 金属氧化物一定是碱性氧化物 | |
| C. | 1L水中溶解58.5g NaCl,该溶液中NaCl的物质的量浓度为1 mol•L-1 | |
| D. | 胶体区别于其他分散系的本质特征是能够产生丁达尔效应 |
分析 A.应选择250mL容量瓶,根据n=cV计算硫酸铜的物质的量,而硫酸铜物质的量与胆矾的相等,再根据m=nM计算胆矾的质量;
B.金属氧化物可以是两性氧化物或酸性氧化物;
C.58.5g NaCl物质的量为1mol,溶于水配成1L溶液,所得溶液浓度为1mol/L;
D.胶体区别于其他分散系的本质特征是分散质微粒直径大小.
解答 解:A.应选择250mL容量瓶,硫酸铜的物质的量为0.25L×0.1mol/L=0.025mol,而硫酸铜物质的量与胆矾的相等,需要胆矾的质量为0.025mol×250g/mol=6.25g,约是6.3g,故A正确;
B.金属氧化物可以是两性氧化物或酸性氧化物,如氧化铝属于两性氧化物,Mn2O7属于酸性氧化物,故B错误;
C.58.5g NaCl物质的量为1mol,溶于水配成1L溶液,所得溶液浓度为1mol/L,故C错误;
D.胶体区别于其他分散系的本质特征是分散质微粒直径大小,故D错误,
故选:A.
点评 本题考查物质的量浓度计算及配制、氧化物、胶体等,注意常见容量瓶规格,理解物质的量浓度定义.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
1.正确掌握好化学用语是学好化学的基础,下列有关表述正确的是( )
| A. | 质量数为16的氧原子:${\;}_{16}^{8}$O | |
| B. | 苛性钠化学式:Na2CO3 | |
| C. | 镁离子结构示意图: | |
| D. | 次氯酸钠在水中电离:NaClO═Na++Cl-+O2- |
2.下列离子方程式改写成化学方程式正确的是( )
| A. | Cu2++2OH-═Cu(OH)2↓ CuCO3+2NaOH═Cu(OH)2↓+Na2CO3 | |
| B. | CO32-+2H+═CO2↑+H2O BaCO3+2HCl═BaCl2+CO2↑+H2O | |
| C. | Ca2++CO32-═CaCO3↓ Ca(NO3)2+Na2CO3═CaCO3↓+2NaNO3 | |
| D. | H++OH-═H2O Ba(OH)2+H2SO4═BaSO4+2H2O |
10.化学与生活息息相关,下列说法错误的是( )
| A. | 乙烯可作为水果的催熟剂 | |
| B. | 用二氧化碳制全降解塑料,可以缓解温室效应 | |
| C. | 氧化铝陶瓷和光导纤维都属于无机非金属材料 | |
| D. | 丙烷(C3H8)和乙醇(C2H5OH)均存在同分异构体 |
20.已知室温下,0.1mol•L-1某一元酸HA在水中有0.1%发生电离,下列叙述错误的是( )
| A. | HA电离出的c(H+)与水电离出的c(H+)之比为108 | |
| B. | 升高温度,溶液的pH减小 | |
| C. | 溶液的pH=4 | |
| D. | HA的电离平衡常数约为l×10-7 |
7.“分类”是一种思想方法,在化学发展中起到了重要的作用.下列分类正确的是( )
| A. | 铁红属于盐类 | B. | 明矾属于碱类 | ||
| C. | SiO2属于酸性氧化物 | D. | NaHCO3属于酸类 |
4.市场上出售的饮料各种各样,有不法商贩为增加饮料口感和粘稠度,在饮料中加塑化剂,塑化剂的分子式为C16H22O4,不能作为食品添加剂.塑化剂属于( )
| A. | 单质 | B. | 氧化物 | C. | 无机物 | D. | 有机物 |
5.有关物质的分类,下列说法错误的是( )
| A. | 只能有一种分类标准 | B. | 分类标准不同,物质所属类别不同 | ||
| C. | 可能有多种分类标准 | D. | 一种分类标准对应一种分类结果 |
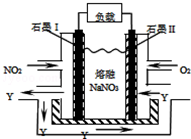 碳和氮的许多化合物在工农业生产和生活中有重要的作用.
碳和氮的许多化合物在工农业生产和生活中有重要的作用.