题目内容
19.利用如图装置探究温度对氨气还原Fe203的影响(固定装置略).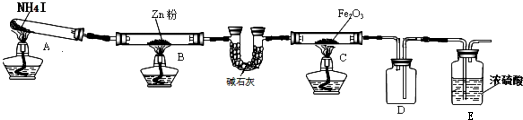
(1)实验时A中有大量紫红色的烟气,则NH4I的分解产物为NH3、H2、I2(HI)(至少填三种),碱石灰的作用是干燥及吸收酸性气体
(2)装置B中的反应化学方程式Zn+I2═ZnI2,D装置的作用是安全瓶,按上图装置进行对比实验,甲组用酒精灯、乙组用酒精喷灯对装置C加热,反应产物均为黑色粉末(纯净物),两组分别用各自的产物进行以下探究,完成下列填空:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无明显变化 |
| 3 | 向步骤2溶液中滴加新制氯水 | 红色先变深后褪去 | 先变红后也褪色 |
(4)步骤1甲组中反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O;
(5)步骤3乙组中溶液变红的原因为Fe2+被氧化为Fe3+,Fe3+遇SCN-显红色,
(6)若装置C中反应后的固体是Fe203和Fe0组成的混合物.为确定其组成.取样品7.84克,在加热条件下通入氨气,完全反应后,停止加热,反应管中铁粉冷却后,称得质量为5.6克,则混合物中Fe203和Fe0的物质的量之比为2:1.
分析 装置A中碘化铵加热分解,实验时A中有大量紫红色的烟气,得到碘单质、氨气、氢气、碘化氢等,通过装置B中 的锌加热反应吸收碘蒸气生成ZnI2,剩余气体通过碱石灰吸收水蒸气和HI,进入装置C中玻璃管加热氢气还原氧化铁反应,生成的气体进入装置D是安全瓶,防止倒吸,最后进入装置E的浓硫酸吸收多余的氨气,
(1)实验时中A有大量紫红色的烟气,说明生成了碘蒸气,NH4I发生下列反应:NH4I(固)?NH3(气)+HI(气),2HI(气)?H2(气)+I2(气),则NH4I的分解产物为 NH3、H2、I2(HI),E装置浓硫酸的作用是 吸收多余的氨气,碱石灰是吸收水蒸气和酸性气体;
(2)装置B中锌的作用是吸收碘蒸气,反应方程式:Zn+I2═ZnI2,故D装置的作用是作安全瓶,防倒吸,因为氨气极易被浓硫酸吸收;
(3)利用黑色固体可溶于盐酸并产生气体,结合“原子守恒”可知用酒精喷灯的乙组实验得到的固体为Fe;
(4)Fe2O3被还原得到黑色固体为Fe3O4,由此可写出反应的离子方程式;
(5)步骤4中溶液变红是溶液中Fe2+被Cl2氧化为Fe3+所致、溶液褪色的原因可能是Cl2将SCN-氧化;
(6)氧化物样品质量为7.84克,还原成铁粉质量为5.6克,设出氧化铁和氧化亚铁的物质的量,分别根据铁的质量、总质量列式计算即可.
解答 解:(1)实验时中A有大量紫红色的烟气,说明生成了碘蒸气,NH4I发生下列反应:NH4I(固)?NH3(气)+HI(气),2HI(气)?H2(气)+I2(气),则NH4I的分解产物为 NH3、H2、I2(HI),碱石灰是吸收水蒸气和酸性气体,
故答案为:NH3、H2、I2(HI);干燥及吸收酸性气体;
(2)装置B的作用是吸收碘蒸气,反应方程式:Zn+I2═ZnI2,因为氨气极易被浓硫酸吸收,故D装置的作用是作安全瓶,防倒吸,
故答案为:Zn+I2═ZnI2;安全瓶;
(3)利用黑色固体可溶于盐酸并产生气体,结合“原子守恒”可知用酒精喷灯的乙组实验得到的固体为Fe,故答案为:Fe;
(4)利用甲组现象可知Fe2O3与CO在酒精灯加热的条件下,Fe2O3被还原得到黑色固体为Fe3O4,由此可写出反应的离子方程式为Fe3O4+8H+=2Fe3++Fe2++4H2O,
故答案为:Fe3O4+8H+=2Fe3++Fe2++4H2O;
(5)因Fe3+遇SCN-显红色,所以乙组步骤3中溶液变红是溶液中Fe2+被Cl2氧化为Fe3+所致,溶液褪色的原因可能是Cl2将SCN-氧化,
故答案为:Fe2+被氧化为Fe3+,Fe3+遇SCN-显红色;
(6)设氧化铁的物质的量为x,氧化亚铁的物质的量为y,则:160x+72y=7.84、(2x+y)×56=5.6,
联立解得:x=0.04mol、y=0.02mol,
则混合物中Fe2O3和FeO的物质的量之比为:0.04mol:0.02mol=2:1,
故答案为:2:1.
点评 本题考查了铁离子、亚铁离子的检验方法、性质实验方案的设计与评价,题目难度中等,试题综合性较强,注意正确理解、分析题中信息,联系所学的知识进行解答.

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案| A. | K+和Na+ | B. | Al3+和Cl- | C. | OH-和NH4+ | D. | H2S和CH4 |
(1)高铁酸钠(Na2FeO4)是水处理过程中的一种新型净水剂,它的氧化性比高锰酸钾更强,本身在反应中被还原成三价铁离子达到净水的目的.按要求回答下列问题:
高铁酸钠主要通过如下反应制取:2Fe(OH)3+3NaClO+4NaOH═2Na2FeO4+3X+5H2O,则X的化学式NaCl.
(2)氧化铁红颜料跟某些油料混合,可以制成防锈油漆.以黄铁矿为原料制硫酸产生的硫酸渣中含Fe2O3、SiO2、Al2O3、MgO等,用硫酸渣制备铁红(Fe2O3)的过程如下:
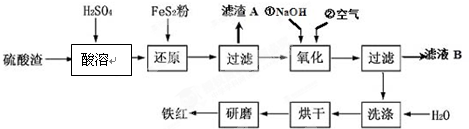
①酸溶过程中Fe2O3与稀硫酸反应的化学方程式为Fe2O3+3H2SO4═Fe2(SO4)3+3H2O;
“滤渣A”主要成份的化学式为SiO2.
②还原过程中加入FeS2的目的是将溶液中的Fe3+还原为Fe2+,而本身被氧化为H2SO4,请完成该反应的离子方程式:FeS2+14Fe3++8H2O═15Fe2++2SO42-+16H+.
③氧化过程中,O2、NaOH与Fe2+反应的离子方程式为4Fe2++O2+2H2O+8OH-=4Fe(OH)3↓.
④为了确保铁红的质量和纯度,氧化过程需要调节溶液的pH的范围是3.2~3.8,如果pH过大,可能引起的后果是Al3+、Mg2+形成沉淀,使制得的铁红不纯(几种离子沉淀的pH见下表);滤液B可以回收的物质有(写化学式)Na2SO4、Al2(SO4)3、MgSO4.
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.8 | 7.6 | 9.4 |
| 完全沉淀pH | 3.2 | 5.2 | 9.7 | 12.4 |
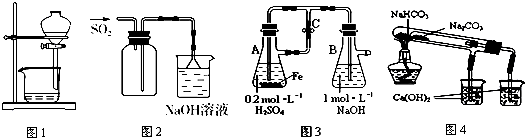
| A. | 图1用于放出碘的苯溶液 | |
| B. | 图2用于实验室收集SO2 | |
| C. | 图3用于实验室制备Fe(OH)2 | |
| D. | 图4用于比较NaHCO3和Na2CO3热稳定性 |
| A. | 温度相同、体积相同的O2和N2 | B. | 质量相等、密度不等的N2和C2H4 | ||
| C. | 体积相同、密度相等的CO和N2O | D. | 压强相同、体积相同的O2和H2 |
| A. | B的阳离子的氧化性比A的阳离子强,则A元素的金属性不一定比B元素强 | |
| B. | 发生氧化还原反应时,A原子失去的电子比B原子多,证明A的金属性一定比B强 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2═2FeCl3+4FeI3 | |
| D. | A的金属性比B的金属性强,则A一定可以在水溶液置换出B来 |
| A. | 金属和酸 | B. | 盐和碱 | C. | 盐和酸 | D. | 酸和碱 |