8.从柑桔中可炼制萜二烯(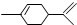 ),下列有关它的推测不正确的是( )
),下列有关它的推测不正确的是( )
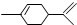 ),下列有关它的推测不正确的是( )
),下列有关它的推测不正确的是( )| A. | 分子式为C10H16 | |
| B. | 常温下呈液态难溶于水 | |
| C. | 所有原子可能共平面 | |
| D. | 与过量溴的CCl4 溶液反应后产物(如图)为: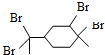 |
7.下列关于同分异构体判断正确的是( )
| A. | 分子式为C3H6Cl2的同分异构体有四种 | |
| B. | 分子式为C8H10的芳香烃有3个,分别为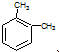 、 、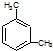 和 和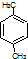 | |
| C. | 分子式为C4H8的烯烃同分异构体有2个,分别为CH2=CHCH2CH3、CH3CH=CHCH3 | |
| D. | 二氯甲烷有两种同分异构体 |
3.很长一段时间认为不存在+7价的溴化合物,直到1968年Appolaman利用下列反应:XeF2+HBrO3+H2O→HBrO4+Xe↑+2HF,首次得到此类化合物.在该反应中作还原剂的物质是( )
| A. | HBrO3 | B. | XeF2 | C. | HBrO4 | D. | Xe |
2.下列不能使碘化钾淀粉试纸变蓝的物质是( )
| A. | 溴水 | B. | 溴化钠 | C. | 氯水 | D. | 碘水 |
1.下列各组中的两种物质发生变化时,所克服的作用力属于同种类型的是( )
| A. | 二氧化硅和氯化镁熔化 | B. | 碘和氯化铵受热变成气体 | ||
| C. | 水和干冰的气化 | D. | 氯化钠和氯化氢溶于水 |
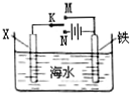
19.利用如图装置探究铁在海水中的电化学防护,下列说法错误的是( )
0 154273 154281 154287 154291 154297 154299 154303 154309 154311 154317 154323 154327 154329 154333 154339 154341 154347 154351 154353 154357 154359 154363 154365 154367 154368 154369 154371 154372 154373 154375 154377 154381 154383 154387 154389 154393 154399 154401 154407 154411 154413 154417 154423 154429 154431 154437 154441 154443 154449 154453 154459 154467 203614

| A. | 若X为锌棒,开关K置于M处,可减缓铁的腐蚀 | |
| B. | 若X为锌棒,开关K置于M处,铁电极的反应:Fe-2e→Fe2+ | |
| C. | 若X为碳棒,开关K置于N处,可减缓铁的腐蚀 | |
| D. | 若X为碳棒,开关K置于N处,铁电极的反应:2H++2e→H2↑ |
 ,违背了泡利不相容原理.
,违背了泡利不相容原理. 由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流 程示意图如下:
由黄铜矿(主要成分是CuFeS2)炼制精铜的工艺流 程示意图如下: