6.下列说法或表示方法中正确的是( )
| A. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由单质A转化为单质B△H=+119kJ/mol,可知单质B比单质A稳定 | |
| C. | 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol | |
| D. | 在25℃、101kPa时,2g H2完全燃烧生成液态水,放出285.8kJ热量,则表示H2燃烧热的化学方程式为2H2(g)+O2(g)=2H2O(l)△H=-571.6kJ/mol |
5.已知2Fe3++2Br-=2Fe2++Br2,当把Cl2通入FeBr2溶液中时,下列离子方程式一定不正确的是( )
| A. | Cl2+2Br-=Br2+2Cl- | |
| B. | 4Cl2+6Br-+2Fe2+=2Fe3++3Br2+8Cl- | |
| C. | 3Cl2+2Fe2++4Br-=2Fe3++2Br2+6Cl- | |
| D. | 2Cl2+2Fe2++2Br-=2Fe3++Br2+4Cl- |
4.已知合成尿素的反应为2NH3(g)+CO2(g)?CO(NH2)2(s)+H2O(g).将体积比为14:13的NH3与CO2的混合气体置于密闭容器中,若反应达到平衡后增大压强,混合气体的平均相对分子质量( )
| A. | 变小 | B. | 不变 | ||
| C. | 增大 | D. | 可能增大、减小,也可能不变 |
3.生活中遇到的某些问题,常常涉及到化学知识.下列各项叙述不正确的是( )
| A. | 鱼虾放久了会产生不愉快的腥臭气味,应当用水冲洗,并在烹调时加人少量食醋 | |
| B. | “酸可除锈”“洗涤剂可去油”都是发生了化学变化 | |
| C. | 被蜂蚁蜇咬会感到疼痛难忍,这是蜂蚁咬人时将甲酸注人人体的缘故,此时若能涂抹稀氨水或碳酸氢钠溶液,可以减轻疼痛 | |
| D. | 煤酚皂溶液可用于环境消毒,医用酒精可用于皮肤消毒,其原因均在于可以使蛋白质发生变性凝固 |
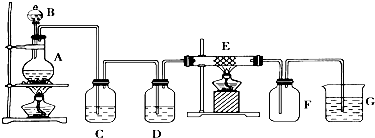
2.氯化亚铜广泛应用于有机合成、染料、颜料、催化剂等工业.氯化亚铜(CuCl)是一种白色粉末,微溶于水、不溶于乙醇、稀硝酸及稀硫酸;可溶于氨水、浓盐酸,并生成配合物NH4[CuCI2];能在空气中迅速被氧化成绿色;见光则分解,变成褐色.如图1是实验室制备氯化亚铜的流程图及实验装置图如图2.

实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36qo盐酸15mL、水.
(1)反应①的化学方程式为NH4[CuCl2]=CuCl↓+NH4Cl,用95%乙醇代替蒸馏水洗涤的主要目的是避免CuCl溶于水而造成损耗,洗去晶体表面的杂质离子及水分.
(2)本实验中通入O2的速率不宜过大,为便于观察和控制产生02的速率,宜选择图3中的B(填字母序号)方案.
(3)实验开始时,温度计显示反应液温度低于室温,主要原因是氯化铵溶于水吸收大量热量;电炉加热升温至50℃时停止加热,反应快速进行,烧瓶上方气体颜色逐渐由无色变为红棕色;当烧瓶上方红棕色气体逐渐变为无色时停止通入氧气,打开瓶塞,沿a或c(填字母)口倾出棕色反应液于l000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出.
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题有防止CuCl被氧化,避光防止分解.
(5)氯化亚铜的定量分析:
①称取样品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;玻璃珠的作用是加速样品的溶解.
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0mol.L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表.
(已知:CuCl+FeCl3═CuCl2+FeCl2,Fe2++Ce4+═Fe3++Ce3+)
④数据处理:计算得CuCI的纯度为95%(平行实验结果相差不能超过0.3%)
0 154210 154218 154224 154228 154234 154236 154240 154246 154248 154254 154260 154264 154266 154270 154276 154278 154284 154288 154290 154294 154296 154300 154302 154304 154305 154306 154308 154309 154310 154312 154314 154318 154320 154324 154326 154330 154336 154338 154344 154348 154350 154354 154360 154366 154368 154374 154378 154380 154386 154390 154396 154404 203614

实验药品:铜丝20g、氯化铵20g、65%硝酸l0mL、36qo盐酸15mL、水.
(1)反应①的化学方程式为NH4[CuCl2]=CuCl↓+NH4Cl,用95%乙醇代替蒸馏水洗涤的主要目的是避免CuCl溶于水而造成损耗,洗去晶体表面的杂质离子及水分.
(2)本实验中通入O2的速率不宜过大,为便于观察和控制产生02的速率,宜选择图3中的B(填字母序号)方案.
(3)实验开始时,温度计显示反应液温度低于室温,主要原因是氯化铵溶于水吸收大量热量;电炉加热升温至50℃时停止加热,反应快速进行,烧瓶上方气体颜色逐渐由无色变为红棕色;当烧瓶上方红棕色气体逐渐变为无色时停止通入氧气,打开瓶塞,沿a或c(填字母)口倾出棕色反应液于l000mL大烧杯中,加水500mL,即刻有大量白色沉淀析出.
(4)在CuCl的生成过程中除环境问题、安全问题外,你认为还应该注意的关键问题有防止CuCl被氧化,避光防止分解.
(5)氯化亚铜的定量分析:
①称取样品0.25g置于预先放入玻璃珠30粒和l0mL过量的FeCl3溶液的250mL锥形瓶中,不断摇动;玻璃珠的作用是加速样品的溶解.
②待样品溶解后,加水50mL,邻菲罗啉指示剂2滴;
③立即用0.l0mol.L-1硫酸铈标准溶液滴至绿色出现为终点并记录读数,再重复实验二次,测得数据如下表.
(已知:CuCl+FeCl3═CuCl2+FeCl2,Fe2++Ce4+═Fe3++Ce3+)
| 实验序号 | 1 | 2 | 3 |
| 滴定起始读数(mL) | 0.75 | 0.50 | 0.80 |
| 滴定终点读数(mL) | 24.65 | 24.75 | 24.70 |
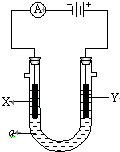 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导与直流电源相连.请回答以下问题:

 ;壬的结构简式
;壬的结构简式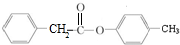


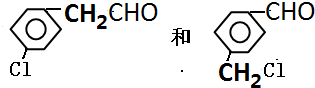 (任写一种)
(任写一种)