17.我国首创的海洋电池以铝板、铂网作电极,海水为电解质溶液,空气中的氧气与铝反应产生电流.电池总反应为:4Al+3O2+6H2O=4A1(OH)3,下列判断错误的是( )
| A. | 铂电极做成网状,可增大与氧气的接触面积 | |
| B. | 该电池通常只需要更换铝板就可继续使用 | |
| C. | 海洋电池中铝板充当负极,发生氧化反应 | |
| D. | 负极反应为:O2+H20+2e-=2OH- |
16.下列关于乙醇的说法正确的是( )
| A. | 与乙酸互为同分异构体 | B. | 属于高分子化合物 | ||
| C. | 不能发生氧化反应 | D. | 可用作燃料 |
15.下列物质中既有离子键又有共价键的是( )
| A. | CaO | B. | CO2 | C. | K2O | D. | Ca(OH )2 |
14.在含有大量的Ba2+、OH-、NO3- 的溶液中还可能大量存在的离子是( )
| A. | Na+ | B. | H+ | C. | SO42- | D. | NH4+ |
13.下列有关胶体与溶液的叙述错误的是( )
| A. | 都是混合物 | B. | 胶体比溶液更隐定 | ||
| C. | 都属于分散系 | D. | 用丁达尔效应区分胶体与溶液 |
12.中美研究人员在新一期美国(环境科学与技术)杂志上报告说,黄粉虫可以吞食和完全降解塑料.他们已在黄粉虫体内分离出靠聚苯乙烯生存的细菌,并将其保存.聚苯乙烯属于( )
| A. | 合金 | B. | 硅酸盐材料 | C. | 有机高分子材料 | D. | 无机非金属材料 |
11.为了改善空气质最,下列措施不合理的是( )
| A. | 减少化石能源的使用,大力发展太阳能、风能等新能源 | |
| B. | 淘汰落后产能,将污染严重的企业从城市迁往农村 | |
| C. | 控制城市机动车持有量,实行机动车限号行驶 | |
| D. | 倡导绿色化学理念,努力实现“原子经济” |
10.已知2mol H2(g)燃烧生成液态水放出的热量为571.6lkJ,而2molH2 (g)完全燃烧生成气态水放的热量为483.6kJ.下列说法正确的是( )
| A. | l molH2O (I)变成lmolH2O (g),向外界释放能量 | |
| B. | 1molH2O (g)分解成H2(g)和O2(g),吸收241. 8kJ能量 | |
| C. | 2mol H2(g)和l mol O2(g)的总能量小于2molH2O(1)的能量 | |
| D. | 断裂2molH2O (g)中所有的O-H键,吸收483.6 kJ能量 |
9.某工厂从废含镍有机催化剂中回收镍的工艺流程如图所示(已知废催化剂中舍有Ni70.0%及一定量的Al、Fe、SiO2和有机物,镍及其化台物的化学性质与铁的类似,但Ni2-的性质较稳定).
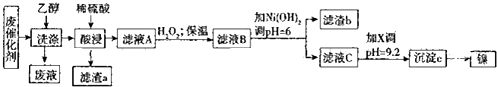
已知:部分阳离子以氢氧化物的形式完全沉淀时的pH如下表所示,回答下列间题
(1)滤渣a的成分是SiO2,用乙醇洗涤废催化剂的目的是溶解、除去有机物,从废渣中回收乙醇的方法是蒸馏.
(2)为提高酸浸速率,可采取的措施有(答两条)将废催化剂粉碎或适当地提高硫酸的浓度、浸泡时的温度.
(3)向A中加人 H2O2时反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O.试剂x可以是蒸馏.
(4)用方程式表示出由沉淀.制取单质镍的方法Ni(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$NiO+H2O、2Al+2NiO $\frac{\underline{\;高温\;}}{\;}$Al2O3+3Ni.回收mkg上述废催化剂的过程中,若将溶液pH调整为6时消耗了akgNi(OH)2,从洗涤到得到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,则最终得到单质镍的质量为(70%×97%m+$\frac{59}{93}$a)×95%kg(填计算式).
(5)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,某化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性条件下发生的反应之一如下,请配平该反应.与电镀相比,化掌镀的最大优点是:不消耗电能,节约能源.

已知:部分阳离子以氢氧化物的形式完全沉淀时的pH如下表所示,回答下列间题
| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 9.2 |
(2)为提高酸浸速率,可采取的措施有(答两条)将废催化剂粉碎或适当地提高硫酸的浓度、浸泡时的温度.
(3)向A中加人 H2O2时反应的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O.试剂x可以是蒸馏.
(4)用方程式表示出由沉淀.制取单质镍的方法Ni(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$NiO+H2O、2Al+2NiO $\frac{\underline{\;高温\;}}{\;}$Al2O3+3Ni.回收mkg上述废催化剂的过程中,若将溶液pH调整为6时消耗了akgNi(OH)2,从洗涤到得到滤液B的过程中镍的损失率为3%,后几步操作过程中镍的损失率为5%,则最终得到单质镍的质量为(70%×97%m+$\frac{59}{93}$a)×95%kg(填计算式).
(5)利用化学镀(待镀件直接置于含有镀层金属的化合物的溶液中)可以在金属、塑料、陶瓷等物品表面镀上一层金属镍或铬等金属,某化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性条件下发生的反应之一如下,请配平该反应.与电镀相比,化掌镀的最大优点是:不消耗电能,节约能源.
8.下列有关氯气的说法正确的是( )
0 154203 154211 154217 154221 154227 154229 154233 154239 154241 154247 154253 154257 154259 154263 154269 154271 154277 154281 154283 154287 154289 154293 154295 154297 154298 154299 154301 154302 154303 154305 154307 154311 154313 154317 154319 154323 154329 154331 154337 154341 154343 154347 154353 154359 154361 154367 154371 154373 154379 154383 154389 154397 203614
| A. | 氯气是黄绿色气体,有毒,有刺激性气味,氯水还可杀菌消毒 | |
| B. | 液氯就是氯气的水溶液,它能使干燥的有色布条褪色 | |
| C. | 红热的铁丝在Cl2中燃烧产生棕色的雾;H2在Cl2中燃烧火焰呈淡蓝色 | |
| D. | 氯水长时间放置会变质,是因为氯气几乎完全挥发,剩下的就是水. |