题目内容
10.已知2mol H2(g)燃烧生成液态水放出的热量为571.6lkJ,而2molH2 (g)完全燃烧生成气态水放的热量为483.6kJ.下列说法正确的是( )| A. | l molH2O (I)变成lmolH2O (g),向外界释放能量 | |
| B. | 1molH2O (g)分解成H2(g)和O2(g),吸收241. 8kJ能量 | |
| C. | 2mol H2(g)和l mol O2(g)的总能量小于2molH2O(1)的能量 | |
| D. | 断裂2molH2O (g)中所有的O-H键,吸收483.6 kJ能量 |
分析 A.根据能量守恒定律分析解答;
B.根据2mol H2(g)完全燃烧生成2mol气态水放出的热量为483.6kJ判断;
C.氢气燃烧为放热反应,反应物总能量大于生成总能量;
D.根据反应热等于反应物总键能减生成物总键能分析解答.
解答 解:A.气态水的能量高于液态水,故1mol H2O(l)变成1mol H2O(g),吸收能量,故A错误;
B.2mol H2(g)完全燃烧生成2mol气态水放出的热量为483.6kJ,则1mol H2O(g)分解成H2(g)和O2(g),吸收241.8 kJ能量,故B正确;
C.氢气燃烧为放热反应,2mol H2(g)和1mol O2(g)的总能量大于2mol H2O(l)的能量,故C错误;
D.2mol H2O(g)分解生成H2(g)和O2(g),吸收483.6 kJ能量,由于反应热等于反应物总键能减生成物总键能,故断裂2mol H2O(g)中所有的O-H键,吸收能量大于483.6kJ,故D错误,
故选B.
点评 本题考查反应热的有关计算,难度不大,注意理解反应热与物质总能量、化学键键能关系.

练习册系列答案
相关题目
20.X、Y、Z、M、W为五种短周期元素.X、Y、Z是原子序数依次递增的同周期元素,且最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状况下的密度为0.76g/L-1;W的质子数是X、Y、Z、M四种元素质子数之和的$\frac{1}{2}$.下列说法正确的是( )
| A. | 元素原子第一电离能大小关系:Z>Y>W>X>M | |
| B. | XZ2、X2M2、W2Z2均为直线形的共价化合物 | |
| C. | Y与M形成化合物键长大于Z与M形成化合物的键长 | |
| D. | 由X、Y、Z、M四种元素形成的化合物一定既有离子键,又有共价键 |
18.常温下,取0.3mol/L HY溶液与0.3mol/L NaOH溶液等体积混合(不计混合后溶液体积变化),测得混合溶液的pH=9,则下列说法(或关系式)正确的是( )
| A. | 混合溶液中由水电离出来的c(OH-)=1×10-9mol/L | |
| B. | c(OH-)-c(HY)=c(H+)=1×10-5mol/L | |
| C. | 混合溶液中c(Na+)=c(Y-)+c(HY)=0.15mol/L | |
| D. | 混合溶液中离子浓度大小次序为:c(Y-)>c(Na+)>c(OH-)>c(H+) |
15.下列物质中既有离子键又有共价键的是( )
| A. | CaO | B. | CO2 | C. | K2O | D. | Ca(OH )2 |
19.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 在某密闭容器中加入0.5molN2和1.5molH2,充分反应后容器中物质含有的N-H键数为3NA | |
| B. | 标准状况下,2.24LSO3含有的原子数为0.4 NA | |
| C. | 71g氯气与足量铁反应过程中转移的电子数为2NA | |
| D. | 电解饱和食盐水时,当阴极产生22.4LH2时,电路中转移的电子数为2NA |


 ;壬的结构简式
;壬的结构简式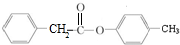


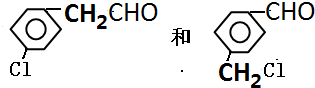 (任写一种)
(任写一种)