2.下列各化合物不能有化合反应生成的是( )
| A. | FeCl2 | B. | Fe(OH)3 | C. | Fe(OH)2 | D. | FeCl3 |
20.能正确表示下列反应的离子方程式的是( )
| A. | 向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:3Ba2++3SO42-+2Al3++6OH-═2BaSO4↓+2Al(OH)3↓ | |
| B. | 醋酸除去水垢:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 碳酸氢钠和偏铝酸钠反应:HCO3-+AlO2-+H2O═CO32-+Al(OH)3↓ | |
| D. | 向硫酸铜中加入过量氨水:Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+ |
19.NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 2L 0.5mol•L-1硫酸钾溶液中阴离子所带电荷数为NA | |
| B. | 室温下,1L pH=13的NaOH溶液中,由水电离的OH-数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 0.1mol 对苯二甲酸中含有双键的数目为0.2NA |
18.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | Na2S | B. | Cl2 | C. | CO2 | D. | NaHCO3 |
16.食盐中的抗结剂是亚铁氰化钾,其化学式为K4[Fe(CN)6]•3H2O2g K4[Fe(CN)6]•3H2O(M=422g/mol)样品受热脱水过程的热重曲线(样品质量随温度的变化曲线)如图1所示.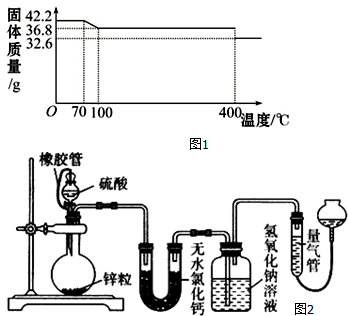
(1)试确定150℃时固体物质的化学式为K4[Fe(CN)6].
(2)在25℃下,将a mol•L-1的KCN(pH>7)溶液与0.01mol•L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a>0.01mol•L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=(100a-1)×10-7 mol•L-1.
(3)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O═2H2SO4的转化.已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
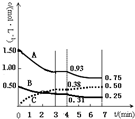
(4)不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图2装置进行实验(实验时压强为10lkPa,温度为0℃).
(Ⅰ)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中n(H2)=(cV-$\frac{m}{32}$)mol(用含字母的代数式表示).若撤走盛有无水氯化钙的U型管,n(SO2):n(H2)的数值将偏大(填偏大、偏小或无影响)
(Ⅱ)在硫酸中加入硫酸铜可以加快氢气的生成速率的原因:锌和铜构成原电池,加快反应速率
(Ⅲ)为进一步探究硫酸铜的量对氢气生成速率的影响,某同学设计如下一系列实验,将表中所给的混合溶液分别加入到5个盛有过量Zn粒的反应瓶中.
①完成此实验设计,其中V5=5,V7=9
②为探究氢气生成速率要收集产生的气体,还需记录:收集等体积气体所需时间.

(1)试确定150℃时固体物质的化学式为K4[Fe(CN)6].
(2)在25℃下,将a mol•L-1的KCN(pH>7)溶液与0.01mol•L-1的盐酸等体积混合,反应平衡时,测得溶液pH=7,则KCN溶液的物质的量浓度a>0.01mol•L-1(填“>”、“<”或“=”);用含a的代数式表示HCN的电离常数Ka=(100a-1)×10-7 mol•L-1.
(3)在Fe2+、Fe3+的催化作用下,可实现2SO2+O2+2H2O═2H2SO4的转化.已知,含SO2的废气通入Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+═4Fe3++2H2O,则另一反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+.
(4)不同浓度的硫酸与锌反应时,硫酸可以被还原为SO2,也可被还原为氢气.为了验证这一事实,某同学拟用如图2装置进行实验(实验时压强为10lkPa,温度为0℃).
(Ⅰ)若在烧瓶中投入d g锌,加入一定量的c mol/L 浓硫酸V L,充分反应后锌有剩余,测得氢氧化钠洗气瓶增重mg,则整个实验过程产生的气体中n(H2)=(cV-$\frac{m}{32}$)mol(用含字母的代数式表示).若撤走盛有无水氯化钙的U型管,n(SO2):n(H2)的数值将偏大(填偏大、偏小或无影响)
(Ⅱ)在硫酸中加入硫酸铜可以加快氢气的生成速率的原因:锌和铜构成原电池,加快反应速率
(Ⅲ)为进一步探究硫酸铜的量对氢气生成速率的影响,某同学设计如下一系列实验,将表中所给的混合溶液分别加入到5个盛有过量Zn粒的反应瓶中.
| 实验 溶液 | A | B | C | D | E |
| 5mol/LH2SO4 mL | 40 | V1 | V2 | V3 | V4 |
| 饱和CuSO4液 mL | 0 | 1 | 2 | V5 | 10 |
| H2O mL | V6 | V7 | V8 | 5 | 0 |
②为探究氢气生成速率要收集产生的气体,还需记录:收集等体积气体所需时间.
15.欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫.请运用化学反应原理的相关知识研究碳及其化合物的性质.
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
5 C+4 KMnO4+6 H2SO4→5CO2↑+4MnSO4+2K2SO4+6H2O
(2)焦炭可用于制取水煤气.测得12g 碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量.该反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g)△H=+131.6kJ•mol-1.
(3)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)$?_{加热}^{催化剂}$CH3OH(g)△H=akJ/mol
如表所列数据是反应在不同温度下的化学平衡常数(K).
①判断反应达到平衡状态的依据是BD
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的平均相对分子质量不变
C.混合气体的密度不变 D.CH3OH、CO、H2的浓度都不再发生变化
②借助上表数据判断,要同时提高CO的转化率和反应的速率,可采取的措施是B
A.升温B.充入H2 C.分离出甲醇D.加入催化剂
③某温度下,将2mol CO和一定量的H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则以H2表示的反应速率v(H2)=0.16mol/(L•min).
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用 Li2CO3和Na2CO3 的熔融盐混合物作电解质,CO 为负极燃气,空气与 CO2 的混和气为正极助燃气,制得在 650℃下工作的燃料电池,其正极反应式:O2+2CO2+4e-=2 CO32-,则 负极反应式:2CO+2CO32--4e-═4CO2
(5)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生反应:BaSO4(s)+CO32-(aq)═BaCO3(s)+SO42-(aq).已知某温度下该反应的平衡常数K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积Ksp=2.5×10-9.
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
5 C+4 KMnO4+6 H2SO4→5CO2↑+4MnSO4+2K2SO4+6H2O
(2)焦炭可用于制取水煤气.测得12g 碳与水蒸气完全反应生成水煤气时,吸收了131.6kJ热量.该反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g)△H=+131.6kJ•mol-1.
(3)工业上在恒容密闭容器中用下列反应合成甲醇:CO(g)+2H2(g)$?_{加热}^{催化剂}$CH3OH(g)△H=akJ/mol
如表所列数据是反应在不同温度下的化学平衡常数(K).
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
A.生成CH3OH的速率与消耗CO的速率相等 B.混合气体的平均相对分子质量不变
C.混合气体的密度不变 D.CH3OH、CO、H2的浓度都不再发生变化
②借助上表数据判断,要同时提高CO的转化率和反应的速率,可采取的措施是B
A.升温B.充入H2 C.分离出甲醇D.加入催化剂
③某温度下,将2mol CO和一定量的H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则以H2表示的反应速率v(H2)=0.16mol/(L•min).
(4)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用 Li2CO3和Na2CO3 的熔融盐混合物作电解质,CO 为负极燃气,空气与 CO2 的混和气为正极助燃气,制得在 650℃下工作的燃料电池,其正极反应式:O2+2CO2+4e-=2 CO32-,则 负极反应式:2CO+2CO32--4e-═4CO2
(5)向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生反应:BaSO4(s)+CO32-(aq)═BaCO3(s)+SO42-(aq).已知某温度下该反应的平衡常数K=4.0×10-2,BaSO4的Ksp=1.0×10-10,则 BaCO3的溶度积Ksp=2.5×10-9.
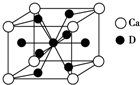
14. 有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )
有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )
 有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )
有A、B、C三种气体在一个固定容积的容器中发生反应,体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )| A. | 该反应的化学方程式为3A(g)+B(g)═2C(g) | |
| B. | 若将初始投放的物质浓度增至原来的2倍,则反应物的转化率增大,平衡常数不变 | |
| C. | 若第4 min 时降低温度,到7 min时达到了新的平衡,则此反应的△H<0 | |
| D. | 反应在前3 min的平均反应速率υ(A)=0.31mol•L-1•min-1 |
13.某短周期金属元素原子核外最外层电子数是最内层电子数的1.5倍,下列说法正确的是( )
0 154053 154061 154067 154071 154077 154079 154083 154089 154091 154097 154103 154107 154109 154113 154119 154121 154127 154131 154133 154137 154139 154143 154145 154147 154148 154149 154151 154152 154153 154155 154157 154161 154163 154167 154169 154173 154179 154181 154187 154191 154193 154197 154203 154209 154211 154217 154221 154223 154229 154233 154239 154247 203614
| A. | 该元素的单质性质活泼,具有较强的还原性,可以用于某些金属冶炼 | |
| B. | 该元素的单质常温下不与浓硫酸反应 | |
| C. | 该元素的单质无需特别保存,因为其性质稳定,不易与空气成分反应 | |
| D. | 该元素的最高价氧化物对应的水化物只能与酸反应 |
 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题: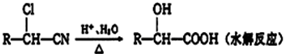
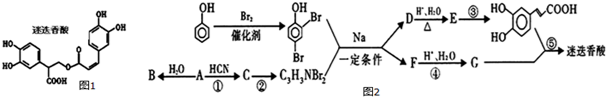
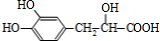 $→_{△}^{浓硫酸}$
$→_{△}^{浓硫酸}$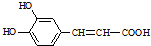 +H2O
+H2O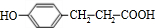 .
.