题目内容
13.某短周期金属元素原子核外最外层电子数是最内层电子数的1.5倍,下列说法正确的是( )| A. | 该元素的单质性质活泼,具有较强的还原性,可以用于某些金属冶炼 | |
| B. | 该元素的单质常温下不与浓硫酸反应 | |
| C. | 该元素的单质无需特别保存,因为其性质稳定,不易与空气成分反应 | |
| D. | 该元素的最高价氧化物对应的水化物只能与酸反应 |
分析 短周期金属元素原子核外最外层电子数是最内层电子数的1.5倍,最外层电子数为3,则该元素为Al.
A.Al单质还原性强,利用铝热反应可以冶炼金属;
B.Al在浓硫酸中发生钝化;
C.表面形成致密的氧化物保护膜;
D.氢氧化铝属于两性氢氧化物.
解答 解:短周期金属元素原子核外最外层电子数是最内层电子数的1.5倍,最外层电子数为3,则该元素为Al.
A.Al单质还原性强,利用铝热反应可以冶炼金属,故A正确;
B.Al在浓硫酸生成致密的氧化物保护膜,阻止内部金属与硫酸反应发生钝化,故B错误;
C.Al的表面形成致密的氧化物保护膜,单质无需特别保存,故C错误;
D.氢氧化铝属于两性氢氧化物,能与强酸、强碱反应,故D错误,
故选:A.
点评 本题考查原子结构与元素性质,侧重考查Al元素单质化合物的性质,注意对基础知识的理解掌握.

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
3.设NA为阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 1mol•L-1MgCl2溶液中的Mg2+数为NA | |
| B. | 1molNa2O2固体中含阴离子总数为2NA | |
| C. | 5g质量分数为46%的乙醇溶液中,氢原子的总数为0.6NA | |
| D. | 100mL12mol•L-1浓盐酸与足量MnO2加热反应,转移电子数为1.2NA |
4.除杂(括号内为杂质),请把所加试剂和有关离子方程式填在空白处.
| 试剂 | 离子方程式 | |
| ①NaCl (Na2SO4) | ||
| ②NaCl(MgCl2) | ||
| ③NaCl(Na2CO3) |
18.下列物质的水溶液能导电,但属于非电解质的是( )
| A. | Na2S | B. | Cl2 | C. | CO2 | D. | NaHCO3 |
5.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 4gNaOH固体所含电子总数为2NA | |
| B. | 22.4lL C2H6所含化学键总数为7 NA | |
| C. | 6g SiO2所含分子数为0.1NA,化学键总数为0.4 NA | |
| D. | 0.1 mol•L-1NH4Cl溶液中,NH${\;}_{4}^{+}$与Cl-数之和小于0.2NA |
2.某有机物和过量钠反应生成气体VaL,另一份等质量的该有机物和碳酸氢钠反应生成VbL气体(同温同压),若Va=Vb,则该有机物可能是( )
| A. | HOCH2CH2COOH | B. | CH3COOH | ||
| C. | HOOC-COOH | D. | 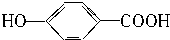 |