2.用下列试剂或方法不能鉴别NaCl溶液和KOH溶液的是( )
| A. | 无色酚酞试液 | B. | Ba(NO3)2溶液 | C. | CuCl2溶液 | D. | 焰色反应 |
1.过氧化尿素是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域.湿法工艺制取过氧化尿素是用低浓度的双氧水和饱和尿素溶液在一定条件下合成过氧化尿素.反应的方程式为:CO(NH2)2+H2O2$\frac{\underline{\;30℃\;}}{\;}$CO(NH2)2•H2O2△H<0.过氧化尿素的部分性质如下:
湿法合成过氧化尿素的流程图如下:
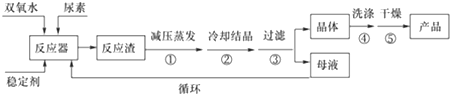
请回答下列问题:
(1)反应器的加热方式是水浴加热;反应温度需控制在适当温度下进行,温度不能过高的原因是温度过高,产品易分解,致使活性氧含量降低,温度也不能过低的原因温度过低,反应速率太慢,且反应体系制冷需要消耗大量能量.
(2)若欲从母液中分离出H2O2和尿素,可采用的操作是减压蒸馏、结晶.
(3)干法工艺制取过氧化尿素的方法是:采用高浓度双氧水水溶液喷雾到无水尿素固体上进行反应,水和反应热通过流态床移去而得到干燥的过氧化尿素产品.
比较干法与湿法两种工艺,你认为干法工艺的优点是:流程短,工艺简单 (答出一点即可),
干法工艺的缺点是:双氧水浓度高经济效益低,设备复杂;技术条件苛刻;产品稳定性差;产品污染不纯等 (答出两点即可),
湿法工艺的优点是:低浓度双氧水,经济效益高;设备简单易于达到;能耗低;产品稳定性好;母液可循环使用等 (答出两点即可).
(4)准确称取0.6000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol•L-1 H2SO4,用0.1000mol•L-1 KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2•H2O2的质量分数为78.3% (结果保留到小数点后一位).
| 分子式 | 外观 | 热分解温度 | 熔点 | 溶解性 |
| CO(NH2)2•H2O2 | 白色晶体 | 45℃ | 75-85℃ | 易溶于水、有机溶剂 |

请回答下列问题:
(1)反应器的加热方式是水浴加热;反应温度需控制在适当温度下进行,温度不能过高的原因是温度过高,产品易分解,致使活性氧含量降低,温度也不能过低的原因温度过低,反应速率太慢,且反应体系制冷需要消耗大量能量.
(2)若欲从母液中分离出H2O2和尿素,可采用的操作是减压蒸馏、结晶.
(3)干法工艺制取过氧化尿素的方法是:采用高浓度双氧水水溶液喷雾到无水尿素固体上进行反应,水和反应热通过流态床移去而得到干燥的过氧化尿素产品.
比较干法与湿法两种工艺,你认为干法工艺的优点是:流程短,工艺简单 (答出一点即可),
干法工艺的缺点是:双氧水浓度高经济效益低,设备复杂;技术条件苛刻;产品稳定性差;产品污染不纯等 (答出两点即可),
湿法工艺的优点是:低浓度双氧水,经济效益高;设备简单易于达到;能耗低;产品稳定性好;母液可循环使用等 (答出两点即可).
(4)准确称取0.6000g产品于250mL锥形瓶中,加适量蒸馏水溶解,再加1mL 6mol•L-1 H2SO4,用0.1000mol•L-1 KMnO4标准溶液滴定至终点时消耗20.00mL(尿素与KMnO4溶液不反应),则产品中CO(NH2)2•H2O2的质量分数为78.3% (结果保留到小数点后一位).
20.2009联合国气候变化大会在哥本哈根经过马拉松式的艰难谈判,当地时间12月19日下午达成不具法律约束力的《哥本哈根协议》.下列措施不符合节能减排的是( )
| A. | 大力发展火力发电,解决电力紧张问题 | |
| B. | 在屋顶安装太阳能热水器为居民提供生活用热水 | |
| C. | 为了减少二氧化硫和二氧化氮的排放,工业废气排放到大气之前必须回收处理 | |
| D. | 用杂草、生活垃圾等有机废弃物在沼气池中发酵产生沼气,作家庭燃气 |
19.分类法是研究化学的一种方法,下列乙中的物质与甲的分类关系匹配的是( )
| 选项 | 甲 | 乙 |
| A | 干燥剂 | 浓硫酸、石灰石、无水氯化钙 |
| B | 电解质 | 冰醋酸、铝、水 |
| C | 酸性氧化物 | 二氧化碳、二氧化硫、三氧化硫 |
| D | 碱性氧化物 | 三氧化铁、氧化钠、氧化铝 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
18.有一种星际分子,其分子结构模型如图所示(图中球与球之间的连线代表化学键,如单键、双键、叁键等,不同花纹的球表示不同的原子).对该物质判断正确的是( )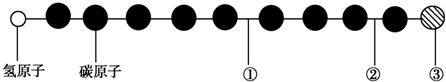

| A. | 该物质是烃的含氧衍生物 | B. | ①处的化学键是碳碳双键 | ||
| C. | ②处的化学键是碳碳单键 | D. | ③处的原子可能是氯原子或氟原子 |
17.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容,据此判断下列说法错误的是( )

| A. | 该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管 | |
| B. | 取10mL该硫酸于烧杯中,再加18.4mL的水可配得9%的硫酸 | |
| C. | 配制200mL 4.6 mol/L的稀硫酸需取该硫酸50mL | |
| D. | 该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2mol/L |
16.下列叙述正确的是(设NA为阿伏加德罗常数的数值)( )
| A. | 检验溶液中是否含有Fe2+的方法是先滴加氯水,再滴加KSCN溶液 | |
| B. | 标准状况下,将11.2LNO2和11.2LN2O4的混合,所得化合物所含分子数为NA | |
| C. | Na2CO3溶液加水稀释后,恢复至原温度,溶液的pH和Kw均减小 | |
| D. | 某电池的总反应为5MnO2+2Ag+2NaCl═Na2Mn5O10+2AgCl,每生成lmolNa2Mn5O10转移电子数2NA |
14.粗CuO是将工业废铜、废电线及废铜合金高温焙烧而成的,杂质主要是铁的氧化物及泥沙,以粗CuO为原料制备CuSO4•5H2O的主要步骤如下图所示:
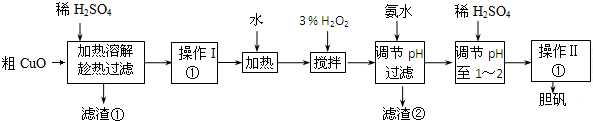
已知:Fe3+、Fe2+、Cu2+转化为氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
(1)写出CuO溶解时的离子方程式CuO+2H+=Cu2++H2O.滤渣②的成分是Fe(OH)3.
(2)加入3% H2O2之前需将热溶液冷却,其目的是防止双氧水分解;加入H2O2后,发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)加入2mol/L氨水后,溶液的pH应在3.2~4.7范围内.
(4)经过操作Ⅰ得到粗胆矾,经过操作Ⅱ得到精制胆矾.两步操作相同,都包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤.其中“洗涤”的目的是洗去表面的杂质离子.

已知:Fe3+、Fe2+、Cu2+转化为氢氧化物时,开始沉淀和沉淀完全时的pH如下表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物沉淀完全时的pH | 3.2 | 9.0 | 6.7 |
(2)加入3% H2O2之前需将热溶液冷却,其目的是防止双氧水分解;加入H2O2后,发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)加入2mol/L氨水后,溶液的pH应在3.2~4.7范围内.
(4)经过操作Ⅰ得到粗胆矾,经过操作Ⅱ得到精制胆矾.两步操作相同,都包括蒸发浓缩、冷却结晶、过滤、洗涤、干燥等步骤.其中“洗涤”的目的是洗去表面的杂质离子.
13.下列反应中,调节反应物用量不会改变反应产物的是( )
0 154045 154053 154059 154063 154069 154071 154075 154081 154083 154089 154095 154099 154101 154105 154111 154113 154119 154123 154125 154129 154131 154135 154137 154139 154140 154141 154143 154144 154145 154147 154149 154153 154155 154159 154161 154165 154171 154173 154179 154183 154185 154189 154195 154201 154203 154209 154213 154215 154221 154225 154231 154239 203614
| A. | CO2通入澄清石灰水中 | B. | 稀硝酸中加入铜片 | ||
| C. | 稀硝酸中加入铁屑 | D. | HCl溶液滴入Na2CO3溶液中 |