7.下列离子方程式中书写正确的是( )
| A. | 固体氯化铵和消石灰混合并加热 NH4++OH-═MH3↑+H20 | |
| B. | 氨水通人过量的二氧化碳 NH3•H20+CO2═NH4++HCO3- | |
| C. | 磷酸二氢钙溶液中加入过量的氢氧化钙 2H2PO4-+3Ca2++40H-═Ca3(PO4)2↓+4H2O | |
| D. | 硫化亚铁与盐酸反应 S2-+2H+═H2S↑ |
6.下列离子方程式正确的是( )
| A. | 用FeCl3溶液腐蚀铜板:Fe3++2Cu═Fe2++2Cu2+ | |
| B. | 向1 mol/L硝酸溶液中加入铜片:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | 在明矾溶液中滴加过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 向小苏打溶液中加少量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
5.下列能达到实验目的是( )


| A. | 图①用于除Cl2中混有的HCl气体 | |
| B. | 图②可用于制取并收集少量NO2气体 | |
| C. | 图③所示实验装置可用排空气法收集CO2 | |
| D. | 图④所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
3.下列实验中,所采取的实验操作或方法与对应的原理均正确的是( )
| 选项 | 实验目的 | 实验操作或方法 | 实验的原理 |
| A | 除去KNO3固体中的NaCl | 滴加过量的AgNO3溶液,过滤,蒸发,干燥 | Cl-+Ag+=AgCl↓ |
| B | 检验NaI中含有I- | 滴加淀粉溶液 | 碘遇淀粉变蓝色 |
| C | 制备FeCl2粉末 | 加热条件下向过量铁粉中通入少量Cl2 | 过量的Fe与Cl2反应生成产物是FeCl2 |
| D | 分离乙酸乙酯和乙醇 | 加入饱和碳酸钠溶液,分液、蒸馏 | 乙酸乙酯和乙醇在饱和碳酸钠溶液中溶解度不同及乙醇沸点低 |
| A. | A | B. | B | C. | C | D. | D |
2.配制溶质质量分数一定的氯化钠溶液涉及的操作有:①称量 ②溶解 ③计算,其正确的操作顺序为( )
| A. | ②①③ | B. | ②③① | C. | ③①② | D. | ③②① |
1.配制一定量浓度的Na2CO3溶液,下列操作说法正确的是( )
| A. | 称量时,把Na2CO3固体直接放在托盘天平的右盘上 | |
| B. | 将Na2CO3固体在烧杯中溶解,所得溶液冷却到室温,再转移至容量瓶中 | |
| C. | 定容时如果加水超过了刻度,用胶头滴管直接吸出多余部分 | |
| D. | 配制溶液时容量瓶中有少量蒸馏水会影响实验结果 |
20.H2CO3和H2C2O4都是二元弱酸,不同pH环境下它们不同形态的粒子的组成百分率如图所示,下列判断正确的是( )


| A. | 在pH为6.37及10.25时,溶液中c(CO32-)=c(HCO3-)=c(H2CO3) | |
| B. | 反应HCO3-+H2O═H2CO3+OH- 的平衡常数为10-10.25 | |
| C. | 0.1mol•L-1NaHC2O4溶液中c(HC2O4-)+c(C2O42-)+c(H2C2O4)=0.1mol•L-1 | |
| D. | 往Na2CO3溶液中加入少量草酸溶液,发生反应:CO32-+H2C2O4═HC2O4-+HCO3- |
18. 向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.其中甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,一段时间后达到平衡时,测得两容器中c(SO2)[mol•L-1]随时间t(min)的变化关系如图所示.下列说法正确的是( )
向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.其中甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,一段时间后达到平衡时,测得两容器中c(SO2)[mol•L-1]随时间t(min)的变化关系如图所示.下列说法正确的是( )
0 153963 153971 153977 153981 153987 153989 153993 153999 154001 154007 154013 154017 154019 154023 154029 154031 154037 154041 154043 154047 154049 154053 154055 154057 154058 154059 154061 154062 154063 154065 154067 154071 154073 154077 154079 154083 154089 154091 154097 154101 154103 154107 154113 154119 154121 154127 154131 154133 154139 154143 154149 154157 203614
 向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.其中甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,一段时间后达到平衡时,测得两容器中c(SO2)[mol•L-1]随时间t(min)的变化关系如图所示.下列说法正确的是( )
向甲、乙两个容积均为1L的恒温恒容的密闭容器中,分别充入一定量的SO2和O2发生反应:2SO2(g)+O2(g)?2SO3(g)△H=-197.74kJ•mol-1.其中甲充入2molSO2、1molO2,乙充入1molSO2、0.5molO2,一段时间后达到平衡时,测得两容器中c(SO2)[mol•L-1]随时间t(min)的变化关系如图所示.下列说法正确的是( )| A. | 压强:p(甲)<2p(乙) | |
| B. | 热量:Q(甲)<2Q(乙) | |
| C. | 乙中前5min内的反应速率v(O2)=0.10mol•L-1•min-1 | |
| D. | 保持其他条件不变,若起始时向乙中充入0.4molSO2、0.2molO2、0.4molSO3,则此时v(正)<v(逆) |
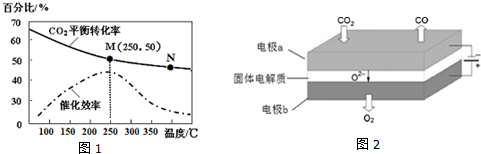
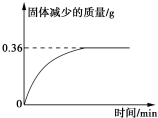 矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示.
矿物透闪石是制作玉器的一种原料,其化学式可用CaxMgySi8O22(OH)m表示.