题目内容
1.配制一定量浓度的Na2CO3溶液,下列操作说法正确的是( )| A. | 称量时,把Na2CO3固体直接放在托盘天平的右盘上 | |
| B. | 将Na2CO3固体在烧杯中溶解,所得溶液冷却到室温,再转移至容量瓶中 | |
| C. | 定容时如果加水超过了刻度,用胶头滴管直接吸出多余部分 | |
| D. | 配制溶液时容量瓶中有少量蒸馏水会影响实验结果 |
分析 A.氢氧化钠具有强腐蚀性,不能直接放在托盘天平的托盘上称量,应该放在小烧杯中快速称量;
B.热的溶液影响溶液体积,需要冷却后再转移到容量瓶中;
C.加水超过了刻度线,配制的溶液体积偏大,此次配制失败,应该出现配制;
D.容量瓶中有少量蒸馏水,对溶质的物质的量及最终溶液体积都无影响.
解答 解:A.由于氢氧化钠具有腐蚀性,且容易潮解,称量氢氧化钠固体时应该放在小烧杯中快速称量,不能直接放在托盘天平的托盘上称量,故A错误;
B.溶解碳酸钠需要在烧杯中进行,由于热的溶液影响溶液体积,则应该冷却后再转移到容量瓶中,故B正确;
C.定容时如果加水超过了刻度线,导致配制的溶液体积偏大,此次配制失败,需要重新配制,不能用胶头滴管直接吸出多余部分,故C错误;
D.配制前容量瓶中有少量蒸馏水,对溶质的物质的量、最终溶液的体积都没有影响,则不影响配制结果,故D错误;
故选B.
点评 本题考查溶液配制的方法,题目难度不大,注意掌握配制一定物质的量浓度的溶液的操作方法,试题侧重基础知识的考查,培养了学生的分析能力及化学实验能力.

练习册系列答案
相关题目
1.将足量的两份铝,分别加入到等物质的量的盐酸和氢氧化钠溶液中,放出气体的物质的量之比为( )
| A. | 3:2 | B. | 2:3 | C. | 1:1 | D. | 1:3 |
12.普伐他汀是一种调节血脂的药物,其结构简式如图所示(未表示出其空间构型).下列关于普伐他汀的性质描述正确的是( )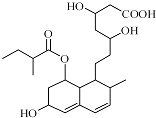

| A. | 该分子中有三种官能团 | B. | 能与FeCl3溶液发生显色反应 | ||
| C. | 能发生加成、取代、消去反应 | D. | 1mol该物质最多可与1molNaOH反应 |
9.X、Y、Z、M、W为原子序数依次增大的5种短周期元素.X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍.Z与其同主族的短周期元素可形成常见气体甲.X、Y、Z 3种元素形成化合物乙.下列说法错误的是( )
| A. | 气体甲可与Z的某种氢化物反应生成强酸 | |
| B. | 化合物乙中一定只有共价键 | |
| C. | W元素的某种单质可在电子工业用于生产半导体材料 | |
| D. | X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM |
16.下列叙述正确的是( )
| A. | 在标准状况下,1 mol任何物质的体积约为22.4 L | |
| B. | 1 mol气体的体积约为22.4 L | |
| C. | 1 mol氖气和1 mol氧气体积相同 | |
| D. | 在标准状况下,1 mol氖气和氯气混合气体(任意体积比)的体积约为22.4 L |
6.下列离子方程式正确的是( )
| A. | 用FeCl3溶液腐蚀铜板:Fe3++2Cu═Fe2++2Cu2+ | |
| B. | 向1 mol/L硝酸溶液中加入铜片:Cu+4H++2NO3-═Cu2++2NO2↑+2H2O | |
| C. | 在明矾溶液中滴加过量氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 向小苏打溶液中加少量Ba(OH)2溶液:HCO3-+Ba2++OH-═BaCO3↓+H2O |
13.丹参素能明显抑制血小板的聚集,其结构如图所示,下列说法错误的是( )


| A. | 丹参素的分子式为C9H9O5 | |
| B. | 丹参素能发生缩聚、消去、氧化反应 | |
| C. | 1 mol丹参素最多可以和4 mol H2发生加成反应 | |
| D. | 丹参素分子中含有手性碳原子 |
10.下列物质属于等电子体的一组是( )
| A. | CO2和NO2- | B. | B3H6N3和C6H6 | C. | F-和Mg | D. | H2O和CH4 |
11.下列说法正确的是( )
| A. | 丙烷、丁烷、正戊烷的沸点依次降低 | |
| B. | 乙二醇、丙氨酸均可发生缩聚反应 | |
| C. | 蔗糖和麦芽糖水解的最终产物都是葡萄糖 | |
| D. | 饱和(NH4)2SO4溶液可导致蛋清液变性凝固 |