3.下列可能大量共存且溶液是无色的离子组是( )
| A. | H+、Na+、NO3-、MnO4- | B. | OH-、Ba2+、Cl-、SO42- | ||
| C. | HCO3-、K+、OH-、NO3- | D. | NO3-、SO42-、K+、Mg2+ |
2.设NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A. | 在常温常压下,11.2 L氧气所含的分子数为0.5NA | |
| B. | 在常温常压下,1molHe的体积为22.4 L | |
| C. | 32 g氧气所含的原子数目为2NA | |
| D. | 在同温同压下,相同体积的任何气体所含的原子数相等 |
1.1molX气体跟amolY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)?bZ(g) 反应达到平衡后,测得X的转化率为50%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的$\frac{3}{4}$,则a和b的数值可能是( )
| A. | a=1,b=2 | B. | a=2,b=1 | C. | a=2,b=2 | D. | a=3,b=2 |
19.废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废旧电池的铜帽(Cu、Zn 总含量约为99%)回收Cu并制备ZnO 的部分实验过程如下:
(1)铜帽溶解时加入H2O2 的目的是Cu+H2O2+H2SO4=CuSO4+2H2O(用化学方程式表示).铜帽溶解完全后,需将溶液中过量的H2O2 除去.除去H2O2 的简便方法是加热至沸.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的浓度.实验操作为:准确量取100mL含有Cu2+的溶液于烧杯中,取溶液20mL加水稀释至100mL,调节溶液pH=3~4,加入过量的KI,用0.1mol/L Na2S2O3标准溶液滴定至终点.上述过程中反应的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2 2S2O32-+I2═2I-+S4O62-
①滴定选用的指示剂为淀粉溶液
②若滴定前溶液中的H2O2 没有除尽,所测定的Cu2+含量将会偏高(填“偏高”、“偏低”或“不变”).
③若滴定中消耗Na2S2O3标准溶液25mL,则原溶液中Cu2+物质的量浓度为0.125mol/L.
(3)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成ZnO22-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0mol•L-1计算).
实验中可选用的试剂:30%H2O2、1.0mol•L-1HNO3、1.0mol•L-1NaOH.
由除去铜的滤液制备ZnO 的实验步骤依次为:
①向滤液中加入30%H2O2,使其充分反应;②滴加1.0mol•L-1NaOH,调节溶液PH约为5(或3.2≤pH<5.9),使Fe3+沉淀完全;③过滤;④向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全;⑤过滤、洗涤、干燥;⑥900℃煅烧.

(1)铜帽溶解时加入H2O2 的目的是Cu+H2O2+H2SO4=CuSO4+2H2O(用化学方程式表示).铜帽溶解完全后,需将溶液中过量的H2O2 除去.除去H2O2 的简便方法是加热至沸.
(2)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)的量,实验中需测定除去H2O2 后溶液中Cu2+的浓度.实验操作为:准确量取100mL含有Cu2+的溶液于烧杯中,取溶液20mL加水稀释至100mL,调节溶液pH=3~4,加入过量的KI,用0.1mol/L Na2S2O3标准溶液滴定至终点.上述过程中反应的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2 2S2O32-+I2═2I-+S4O62-
①滴定选用的指示剂为淀粉溶液
②若滴定前溶液中的H2O2 没有除尽,所测定的Cu2+含量将会偏高(填“偏高”、“偏低”或“不变”).
③若滴定中消耗Na2S2O3标准溶液25mL,则原溶液中Cu2+物质的量浓度为0.125mol/L.
(3)已知pH>11 时Zn(OH)2 能溶于NaOH溶液生成ZnO22-.下表列出了几种离子生成氢氧化物沉淀的pH(开始沉淀的pH 按金属离子浓度为1.0mol•L-1计算).
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
由除去铜的滤液制备ZnO 的实验步骤依次为:
①向滤液中加入30%H2O2,使其充分反应;②滴加1.0mol•L-1NaOH,调节溶液PH约为5(或3.2≤pH<5.9),使Fe3+沉淀完全;③过滤;④向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全;⑤过滤、洗涤、干燥;⑥900℃煅烧.
16.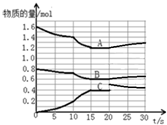 在2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g)△H>0,容器中A、B、C物质的量随反应时间的变化如图所示,下列有关说法不正确的是( )
在2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g)△H>0,容器中A、B、C物质的量随反应时间的变化如图所示,下列有关说法不正确的是( )
 在2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g)△H>0,容器中A、B、C物质的量随反应时间的变化如图所示,下列有关说法不正确的是( )
在2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g)△H>0,容器中A、B、C物质的量随反应时间的变化如图所示,下列有关说法不正确的是( )| A. | 反应在前10s 内v(B)=0.005mol/(L.s) | |
| B. | 方程式计量数a:b:c为2:1:2 | |
| C. | 10 s时改变条件可能是升高温度,20s时平衡逆向进行 | |
| D. | 15~20s间,反应的平衡常数是2.7 |
15.下列说法正确的是( )
| A. | 一定温度下,反应 MgCl2(l)═Mg(l)+Cl2(g)的△H>0、△S>0 | |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| C. | 在H2S溶液中,C(H+)和C(S2-)的比值为2:1 | |
| D. | 1 mol/L和0.1 mol/L的两瓶氨水中c(OH-)之比为10:1 |
14.已知反应可实现燃煤烟气中硫的回收:SO2(g)+2CO(g)?2CO2(g)+S(l)△H<0若反应在恒容的密闭容器中进行,下列有关说法正确的是( )
0 153908 153916 153922 153926 153932 153934 153938 153944 153946 153952 153958 153962 153964 153968 153974 153976 153982 153986 153988 153992 153994 153998 154000 154002 154003 154004 154006 154007 154008 154010 154012 154016 154018 154022 154024 154028 154034 154036 154042 154046 154048 154052 154058 154064 154066 154072 154076 154078 154084 154088 154094 154102 203614
| A. | 平衡前,充入氮气,容器内压强增大,反应速率加快 | |
| B. | 平衡时,其他条件不变,分离出硫,逆反应速率减小 | |
| C. | 平衡时,其他条件不变,升高温度可提高 SO2 的转化率 | |
| D. | 其他条件不变,缩小容器体积,平衡正反应方向移动,该反应的平衡常数不变 |

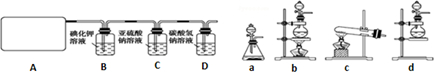
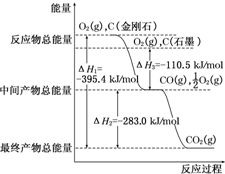 (1)家用液化气中主要成分之一是丁烷(C4H10).当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50kJ.试写出丁烷燃烧反应的热化学方程式
(1)家用液化气中主要成分之一是丁烷(C4H10).当1g丁烷完全燃烧并生成CO2和液态水时,放出热量50kJ.试写出丁烷燃烧反应的热化学方程式