题目内容
15.下列说法正确的是( )| A. | 一定温度下,反应 MgCl2(l)═Mg(l)+Cl2(g)的△H>0、△S>0 | |
| B. | 放热反应的反应速率总是大于吸热反应的反应速率 | |
| C. | 在H2S溶液中,C(H+)和C(S2-)的比值为2:1 | |
| D. | 1 mol/L和0.1 mol/L的两瓶氨水中c(OH-)之比为10:1 |
分析 A、物质的分解反应是吸热反应,根据产物和反应物气体系数和的关系判断反应的熵变;
B、反应速率与反应是吸热还是放热无关;
C、氢硫酸是弱酸,不能完全电离,据此回答;
D、弱电解质溶液中,弱电解质的浓度越大,其电离程度越小,浓度越小,其电离程度越大.
解答 解:A、一定温度下,反应 MgCl2(l)═Mg(l)+Cl2(g)的△H>0,产物气体系数和大于反应物系数和,所以△S>0,故A正确;
B、反应速率与反应是吸热还是放热无关,反应速率与反应物本身的性质及外界条件有关,故B错误;
C、H2S溶液中存在H2S?HS-+H+,HS-?S2-+H+,C(H+)和C(S2-)的比值不是2:1,故C错误;
D、一水合氨是弱电解质,在溶液里存在电离平衡,氨水的浓度越大,一水合氨的电离程度越小,浓度越小,一水合氨的电离程度越大,甲瓶氨水的浓度是乙瓶氨水的浓度的10倍,由弱电解质的浓度越小,电离程度越大,故甲瓶氨水的电离度比乙瓶氨水的电离度小,所以甲、乙两瓶氨水中[OH-]之比小于10,故D错误.
故选:A.
点评 本题考查弱电解质的电离程度与浓度的关系、反应热和焓变的关系等知识,明确一水合氨的电离程度是解答本题的关键,难度中等.

练习册系列答案
相关题目
5.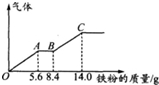 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
 -定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )
-定浓度H2SO4、HNO3混合后的稀溶液100mL,向其中逐渐加人铁粉,产生气体的量随铁粉质量增加的变化如图所示,假设且每一段只对应一个反应,则OA段产生的气体和H2SO4的物质的量浓度分别为( )| A. | NO,1.5mol/L | B. | H2,1.5mol/L | C. | NO,2.5mol/L | D. | H2,2.5mol/L |
3.化学与社会、生产、生活密切相关.下列说法不正确的是( )
| A. | 家用燃气灶是化学能转化为热能的应用装置 | |
| B. | 食品放入冰箱中,因为温度低,变质速率降低,所以食品能够保存较长时间 | |
| C. | 将煤气化,有利于提供更多的能量,而且有效地减少温室气体的产生 | |
| D. | 因为食用醋中含有酸,可以用来清洗锅垢 |
10.将SO2气体通入BaCl2溶液,若要有白色沉淀产生,不可加入(通入)的试剂是( )
| A. | 硝酸溶液 | B. | 二氧化碳 | C. | 氢氧化钠溶液 | D. | 氨水 |
7.下列离子反应方程式正确的是( )
| A. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 将金属Na加入冷水中:2 Na+2 H2O═2 Na++2 OH-+H2↑ | |
| C. | 盐酸滴入澄清石灰水:Ca(OH)2+2 H+═Ca2++2 H2O | |
| D. | 澄清石灰水吸收氯气:Cl2+OH-═Cl-+ClO-+H+ |
4.下列说法中不正确的是( )
| A. | 标准状况下,1.12 L的H2O所含的原子数必大于1.5×6.02×1023 | |
| B. | 含有相同氧原子数的SO2和CO2的物质的量相等 | |
| C. | 常温常压下,48 g O3中含有的氧原子数为3NA | |
| D. | 标准状况下,2.24 L NH3和CH4的混合气体,所含电子总数为2NA |