题目内容
18.某研究性学生小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2CaSO4+2Cl2↑+2H2O.他们设计了如图所示装置制取氯气并验证其性质的实验.
试回答:
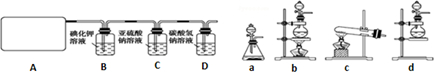
(1)该实验中A部分的装置是b(填写装置的序号).
(2)B中反应的化学方程式是Cl2+2KI=2KCl+I2.
(3)写出C中反应的离子方程式Cl2+SO32-+H2O=SO42-+2Cl-+2H+,并请你帮该小组同学设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):取少量反应后的溶液于试管中,加入HCl溶液至不再产生气体为止,再滴加BaCl2溶液,如果有白色沉淀生成,证明Na2SO3已被氧化.
(4)写出在D装置中发生反应的离子方程式Cl2+H2O?H++Cl-+HClO,HCO3-+H+=H2O+CO2↑或Cl2+HCO3-=CO2↑+Cl-+HClO.
(5)该实验存在明显的缺陷是无尾气处理装置.
分析 (1)根据反应物的状态、反应条件选择发生反应装置.
(2)氯气有氧化性,能和碘化钾反应生成碘单质.
(3)氯气有强氧化性,亚硫酸根离子有还原性,所以氯气和亚硫酸根离子能发生氧化还原反应生成硫酸根离子、氯离子和氢离子;如果亚硫酸钠被氧化会生成硫酸钠,根据硫酸根离子的检验方法检验即可.
(4)氯气和水反应生成盐酸和次氯酸,盐酸能和碳酸氢根离子反应生成二氧化碳.
(5)氯化氢有刺激性气味,尾气不能直接排空,要用尾气处理装置处理.
解答 解:(1)该反应的反应物是固体和液体,反应条件是加热,所以应选固液混合加热型装置,故选b,
故答案为:b;
(2)氯气有氧化性,能和碘化钾反应生成碘单质和氯化钾Cl2+2KI=2KCl+I2.
故答案为:Cl2+2KI=2KCl+I2.
(3)氯气有强氧化性,亚硫酸根离子有还原性,所以氯气和亚硫酸根离子能发生氧化还原反应生成硫酸根离子、氯离子和氢离子Cl2+SO32-+H2O=SO42-+2Cl-+2H+;如果亚硫酸钠被氧化,会生成硫酸钠,硫酸钠和氯化钡能发生 反应生成白色沉淀硫酸钡,亚硫酸钡也是沉淀,所以要先排除亚硫酸盐的干扰,再用氯化钡检验硫酸根离子,检验方法为取少量反应后的溶液于试管中,加入HCl溶液至不再产生气体为止,再滴加BaCl2溶液,如果有白色沉淀生成,证明
Na2SO3已被氧化.
故答案为:Cl2+SO32-+H2O=SO42-+2Cl-+2H+;取少量反应后的溶液于试管中,加入HCl溶液至不再产生气体为止,再滴加BaCl2溶液,如果有白色沉淀生成,证明Na2SO3已被氧化.
(4)氯气和水反应生成盐酸和次氯酸Cl2+H2O?H++Cl-+HClO,盐酸是强酸,能和碳酸氢根离子反应生成二氧化碳和水HCO3-+H+=H2O+CO2↑.
故答案为:Cl2+H2O?H++Cl-+HClO,HCO3-+H+=H2O+CO2↑(或者Cl2+HCO3-=CO2↑+Cl-+HClO ).
(5)氯化氢有刺激性气味,尾气不能直接排空,要用尾气处理装置进行处理,所以该装置没有尾气处理装置.
故答案为:无尾气处理装置.
点评 本题考查了氯气的实验室制法及化学性质,难度不大,注意亚硫酸根离子的检验方法.

 阅读快车系列答案
阅读快车系列答案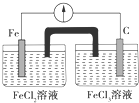
| A. | Fe是负极,C是正极 | B. | 负极反应式:Fe-3e-═Fe3+ | ||
| C. | 内电路中阴离子移向FeCl2溶液 | D. | 电流由石墨电极流向Fe电极 |
| A. | ①②④ | B. | ②③④ | C. | ①③④⑤ | D. | ①②③④ |
| 容器 | SO2(mol) | O2(mol) | N(mol) | Q(kJ) |
| 甲 | 2 | 1 | 0 | Q1 |
| 乙 | 1 | 0.5 | 0 | Q2 |
| 丙 | 1 | 0.5 | 1 | Q3 |
| A. | 在上述条件下反应生成1molSO3气体放热98.5 kJ | |
| B. | Q1=2Q2=2Q3=197 kJ | |
| C. | 上述条件下1mol O2参加反应放出的热量为197 kJ/mol | |
| D. | Q2<Q3<Q1<197kJ |
| A. | H+、Na+、NO3-、MnO4- | B. | OH-、Ba2+、Cl-、SO42- | ||
| C. | HCO3-、K+、OH-、NO3- | D. | NO3-、SO42-、K+、Mg2+ |
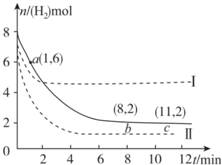 T℃时,6 mol CO2和 8 mol H2充入2 L密闭容器中,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间的变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )
T℃时,6 mol CO2和 8 mol H2充入2 L密闭容器中,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),容器中H2的物质的量随时间的变化如图中实线所示.图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化.下列说法正确的是( )| A. | 反应开始至a点时v(H2)=1 mol•L-1•min-1 | |
| B. | 若曲线Ⅰ对应的条件改变是升温,则该反应△H>0 | |
| C. | 曲线Ⅱ对应的条件改变是减少压强 | |
| D. | T℃时,该反应的化学平衡常数为0.125 |
| A. | 向铁粉中加入一定量的稀硝酸 | |
| B. | 向MgSO4,H2SO4的混合液中滴入过量Ba(OH)2溶液 | |
| C. | 向NaOH溶液中通入一定量CO2气体 | |
| D. | 将物质的量浓度之比为2:7的AlCl3和NaOH溶液等体积混合 |
| A. | 纯碱溶液 | B. | 盐酸 | C. | 硫酸 | D. | 苛性钠溶液 |
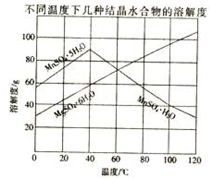 软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2=MnSO4
软锰矿(主要成分MnO2,杂质金属元素Fe、Al、Mg等)的水悬浊液与烟气中SO2反应可制备MnSO4•H2O,反应的化学方程式为:MnO2+SO2=MnSO4