题目内容
16.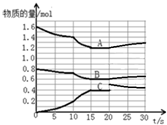 在2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g)△H>0,容器中A、B、C物质的量随反应时间的变化如图所示,下列有关说法不正确的是( )
在2L恒容密闭容器中发生反应aA(g)+bB(g)?cC(g)△H>0,容器中A、B、C物质的量随反应时间的变化如图所示,下列有关说法不正确的是( )| A. | 反应在前10s 内v(B)=0.005mol/(L.s) | |
| B. | 方程式计量数a:b:c为2:1:2 | |
| C. | 10 s时改变条件可能是升高温度,20s时平衡逆向进行 | |
| D. | 15~20s间,反应的平衡常数是2.7 |
分析 A、反应在前10s内,根据v(B)=$\frac{△c}{△t}$来计算;
B、方程式计量数之比等于各物质浓度(物质的量)变化量之比;
C、升高温度,反应正向进行,速率加快,根据影响平衡移动的因素来回答;
D、根据反应的平衡常数K=$\frac{产物平衡浓度系数次幂之积}{反应物平衡浓度系数次幂之积}$来计算.
解答 解:A、反应在前10s内,根据v(B)=$\frac{△c}{△t}$=$\frac{\frac{0.8mol-0.7mol}{2L}}{10s}$=0.005mol/(L.s),故A正确;
B、方程式计量数之比等于各物质浓度(物质的量)变化量之比,方程式计量数a:b:c=(1.6-1.4):(0.8-0.7):(0.2-0)=2:1:2,故B正确;
C、升高温度,反应正向进行,速率加快,20s时,反应物的量逐渐增加,产物的量减少,所以平衡逆向进行,故C正确;
D、反应的平衡常数K=$\frac{产物平衡浓度系数次幂之积}{反应物平衡浓度系数次幂之积}$=$\frac{0.{2}^{2}}{0.{6}^{2}×0.3}$=0.37,故D错误.
故选D.
点评 本题考查了化学反应速率影响因素,化学反应速率、化学平衡常数的计算,图象分析和化学平衡移动原理是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列叙述正确的是( )
| A. | 稀醋酸中加入少量冰醋酸能增大醋酸的电离程度 | |
| B. | 25℃时,等体积等浓度的盐酸与氨水混合后,溶液pH=7 | |
| C. | 0.1 mol AgCl和0.1mol AgI混合后加入1L水中,所得溶液中c(Cl-)=c(I-) | |
| D. | 25℃时,0.1mol•L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱 |
7.25℃时,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=5.1×10-9.在该温度下,下列说法不正确的是( )
| A. | 若误饮c(Ba2+)=1.0×10-5mol/L溶液时,不会引起Ba2+中毒 | |
| B. | 因为Ksp(BaCO3)>Ksp(BaSO4),所以BaCO3不能作内服造影剂 | |
| C. | 向同浓度Na2SO4和Na2CO3的混合溶液中滴加BaCl2溶液,BaSO4先析出 | |
| D. | 在BaSO4和BaCO3共存的悬浊液中,c(SO42-):c(CO32-)=1:51 |
4.有以下仪器:托盘天平、烧杯、漏斗、锥形瓶、药匙、玻璃杯、量筒、酸碱滴定管、铁架台、胶头滴管、容量瓶、环形玻璃搅拌棒,从仪器角度看,不能够完成的实验是( )
| A. | 中和热测定 | B. | 中和滴定 | ||
| C. | 过滤 | D. | 物质的量浓度溶液配制 |
11.下列事实不能用勒夏特列原理解释的是( )
| A. | 氯水中有下列平衡Cl2+H2O═HCl+HClO,当加入硝酸银溶液后,溶液颜色变浅 | |
| B. | 合成氨反应,为提高氨的产率,理论上应采取降低温度的措施 | |
| C. | 氨水中加入NaOH固体有利于氨气的溢出 | |
| D. | pH=1的盐酸加水稀释到原体积的100倍后,PH=3 |
1.1molX气体跟amolY气体在体积可变的密闭容器中发生如下反应:X(g)+aY(g)?bZ(g) 反应达到平衡后,测得X的转化率为50%.而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的$\frac{3}{4}$,则a和b的数值可能是( )
| A. | a=1,b=2 | B. | a=2,b=1 | C. | a=2,b=2 | D. | a=3,b=2 |
8.瓦斯爆炸是空气中含CH45%~15%(体积分数)遇火所产生的.发生爆炸最强烈时,CH4在空气中的体积分数约为( )
| A. | 10.5% | B. | 9.1% | C. | 8% | D. | 5% |
5.下列化学方程式或离子方程式不正确的是( )
| A. | S与Cu反应:Cu+S$\frac{\underline{\;\;△\;\;}}{\;}$CuS | |
| B. | 酸雨放置过程中pH变小:2H2SO3+O2═2H2SO4 | |
| C. | 亚硫酸氢钙溶液与澄清的石灰水混合:Ca2++HSO3-+OH-═CaSO3↓+H2O | |
| D. | 向Na2S和Na2SO3的混合溶液中滴加稀H2SO4[n(Na2S):n(Na2SO3)=2:1]:2S2-+SO32-+6H+═3S↓+3H2O |
19.下列说法正确的是( )
| A. | 除去N2中的O2:通过灼热的CuO粉末,收集气体 | |
| B. | 某吸热反应能自发进行,则该反应一定是熵增的反应 | |
| C. |  如图是从化学试剂商店买回的硫酸试剂标签,配制80mL2.3mol•L-1的稀硫酸需量取该硫酸12.5 mL | |
| D. | 下列各种物质在一定条件下反应,所得产物与反应物的用量或与反应条件无关①Na2SiO3+CO2+H2O ②Fe+Cl2 ③Ca(HCO3)2+Ca(OH)2 |