16.25℃时,向1L浓度均为1mol•L-1的弱酸(HA)及其盐(NaA)组成的混合溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入n(H+)或n(OH-)而变化的曲线如图.下列有关说法错误的是( )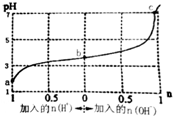

| A. | b点溶液中c(A-)>c(Na+)>c(HA) | |
| B. | 通入HCl后,c(HA)/c(A-)增大 | |
| C. | 当加入1 mol NaOH后,溶液中c(Na+)=c(A-) | |
| D. | a、b、c三点溶液中水的电离程度依次增大 |
15. 在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH的浓度随时间变化如图所示.下列说法正确的是( )
在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH的浓度随时间变化如图所示.下列说法正确的是( )
 在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH的浓度随时间变化如图所示.下列说法正确的是( )
在体积为1L的恒温密闭容器中,充入1molCO2和3molH2,一定条件下发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g),测得CO2和CH3OH的浓度随时间变化如图所示.下列说法正确的是( )| A. | 该化学反应在3min时达到平衡状态 | |
| B. | 保持其他条件不变,降低温度,平衡时c(CH3OH)=0.85 mol•L-1,则该反应的△H<0 | |
| C. | 相同温度下,起始时向上述容器中充入0.5molCO2、1.5molH2,平衡时CO2的转化率小于75% | |
| D. | 12min时,向上述容器中再充入0.25molCO2、0.25molH2O(g),此时反应将向逆反应方向进行 |
14.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | “84”消毒液中:K+、CO32-、Na+、I- | |
| B. | $\frac{K_W}{{C({H^+})}}$=1×10-13mol.L-1的溶液中:NH4+、Ca2+、Cl-、NO3- | |
| C. | 能使PH试纸显蓝色的溶液中:Na+、CH3COO-、Fe3+、SO42- | |
| D. | 通入足量的H2S后的溶液中:Al3+、Cu2+、SO42-、Cl- |
13.短周期主族元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为24.X的原子半径比Y大,Y与Z同主族,Y原子的最外层电子数是电子层数的3倍,下列说法正确的是( )
| A. | Y元素形成的单核阴离子还原性强于X | |
| B. | Z元素的简单气态氢化物的沸点比Y高 | |
| C. | W元素氧化物对应的水化物的酸性一定强于Z | |
| D. | X的气态氢化物可与其最高价含氧酸反应生成离子化合物 |
10.下列离子方程式正确的是( )
| A. | 少量金属钠加到冷水中:Na+2H2O═Na++2OH-+H2↑ | |
| B. | NaHCO3溶液中滴加少量Ca(OH)2溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| C. | 硫酸铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 将2 mol/L AlCl3溶液和7 mol/L NaOH溶液等体积混合:2Al3++7OH-═Al(OH)3↓+AlO2-+2H2O |
9.下列电离方程式正确的是( )
| A. | Ba(OH)2═Ba2++2OH- | B. | AlCl3═Al3++Cl3- | ||
| C. | H2SO4═2H++S6++4O2- | D. | Na2CO3═Na2++CO32- |
8.常温下,下列溶液pH=2的是( )
0 153875 153883 153889 153893 153899 153901 153905 153911 153913 153919 153925 153929 153931 153935 153941 153943 153949 153953 153955 153959 153961 153965 153967 153969 153970 153971 153973 153974 153975 153977 153979 153983 153985 153989 153991 153995 154001 154003 154009 154013 154015 154019 154025 154031 154033 154039 154043 154045 154051 154055 154061 154069 203614
| A. | 0.01 mol•L-1 CH3COOH溶液 | |
| B. | 10-3 mol•L-1 H2SO4浓缩到原体积的10倍. | |
| C. | pH=1的H2SO4溶液稀释10倍 | |
| D. | c(OH-)=10-2 mol•L-1 的某溶液 |
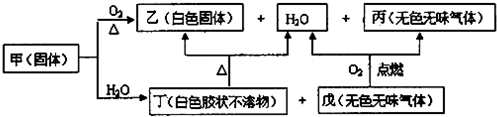

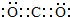 ;
; HClO+OH-;
HClO+OH-; ;1mol O22+中含有的π键数目为2NA.
;1mol O22+中含有的π键数目为2NA.