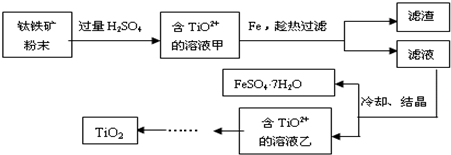
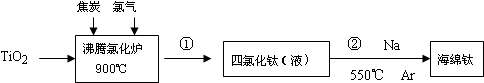
3.一定温度下,向0.1mol•L-1 CH3COOH溶液中加少量水,下列有关说法不正确的是( )
| A. | CH3COOH的电离程度变大 | B. | c(CH3COO-)增大 | ||
| C. | CH3COOH的Ka不变 | D. | 溶液的pH增大 |
2.草酸(H2C2O4)是一种二元弱酸,主要用作还原剂和漂白剂.草酸的盐可用作碱土金属离子的广谱沉淀剂.
(1)草酸的电离方程式:H2C2O4?HC2O4-+H+ HC2O4-?C2O42-+H+.
(2)浓度为0.1mol/L的Na2C2O4溶液中:c(C2O42-)+c(HC2O4-)+c(H2C2O4)=0.1mol/L
(3)40℃时混合一定体积的0.1mol/L H2C2O4溶液与一定体积0.01mol/L酸性KMnO4溶液,填写表中空格.
(4)结晶水合草酸(H2C2O4•2H2O)成品的纯度用高锰酸钾法测定.称量草酸成品0.250g溶于水,用0.0500mol/L的酸性KMnO4溶液滴定,至浅粉红色不消褪,消耗KMnO4溶液15.00mL,反应的离子方程式为:5H2C2O4+2MnO4-+6H+═2Mn2++8H2O+10CO2↑;列式计算该成品的纯度94.5%.
(5)常温下MgC2O4的Ksp=8.1×10-5,已知当溶液中某离子的浓度≤10-5mol/L时可认为该离子已沉淀完全.现为了沉淀1L0.01mol/LMgCl2溶液中的Mg2+,加入100mL0.1mol/L的(NH4)2C2O4溶液,通过计算判断Mg2+是否已沉淀完全(写出计算过程).
(1)草酸的电离方程式:H2C2O4?HC2O4-+H+ HC2O4-?C2O42-+H+.
(2)浓度为0.1mol/L的Na2C2O4溶液中:c(C2O42-)+c(HC2O4-)+c(H2C2O4)=0.1mol/L
(3)40℃时混合一定体积的0.1mol/L H2C2O4溶液与一定体积0.01mol/L酸性KMnO4溶液,填写表中空格.
| 温度 | v(H2C2O4) | v(KMnO4) | KMnO4褪色时间 |
| 40℃ | 10mL | 10mL | 40s |
| 40℃ | 20mL | 20mL |
(5)常温下MgC2O4的Ksp=8.1×10-5,已知当溶液中某离子的浓度≤10-5mol/L时可认为该离子已沉淀完全.现为了沉淀1L0.01mol/LMgCl2溶液中的Mg2+,加入100mL0.1mol/L的(NH4)2C2O4溶液,通过计算判断Mg2+是否已沉淀完全(写出计算过程).
19. 高纯MnCO3是制备高性能磁性材料的主要原料.某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
高纯MnCO3是制备高性能磁性材料的主要原料.某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
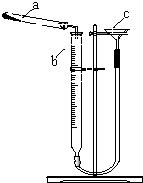
①缓慢向烧瓶中(见图)通入过量混合气进行“浸锰”操作,主要反应原理为:SO2+H2O=H2SO3;MnO2+H2SO3=MnSO4+H2O(铁浸出后,过量的SO2会将Fe3+还原为Fe2+)
②向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末.
③再用Na2CO3溶液调节pH为3.5左右,过滤.
④调节滤液pH为6.5~7.2,加入NH4HCO3,有无色无味的气体放出,同时有浅红色的沉淀生成,经过滤、洗涤、干燥,得到高纯碳酸锰.请回答:
(1)石灰乳参与反应的化学方程式为Ca(OH)2+SO2═CaSO3+H2O.
(2)“浸锰”反应中往往有副产物MnS2O6的生成,温度对“浸锰”反应的影响如下图,为减少MnS2O6 的生成,“浸锰”过程适宜的温度是150℃(或150℃以上).

(3)查阅下表回答②中加入一定量纯MnO2粉末的主要作用是将Fe2+氧化为Fe3+,将过量的SO2氧化除去.
(4)③中所得的滤液中含有Cu2+,可添加过量的难溶电解质MnS除去Cu2+,经过滤,得到纯净的MnSO4溶液.用平衡移动原理解释加入MnS的作用MnS(S)?Mn2+(aq)+S2-(aq)、S2-(aq)+Cu2+(aq)?CuS(S) 生成的CuS比MnS更难溶,促进MnS不断溶解,平衡右移,使Cu2+除去.
(5)④中加入NH4HCO3后发生反应的离子方程式是Mn2++2HCO3-=MnCO3↓+CO2↑+H2O.
(6)已知MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解.请问用少量C2H5OH洗涤的原因是防止MnCO3潮湿时被空气氧化、便于在温度低于100℃干燥等.
 高纯MnCO3是制备高性能磁性材料的主要原料.某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
高纯MnCO3是制备高性能磁性材料的主要原料.某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):①缓慢向烧瓶中(见图)通入过量混合气进行“浸锰”操作,主要反应原理为:SO2+H2O=H2SO3;MnO2+H2SO3=MnSO4+H2O(铁浸出后,过量的SO2会将Fe3+还原为Fe2+)
②向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末.
③再用Na2CO3溶液调节pH为3.5左右,过滤.
④调节滤液pH为6.5~7.2,加入NH4HCO3,有无色无味的气体放出,同时有浅红色的沉淀生成,经过滤、洗涤、干燥,得到高纯碳酸锰.请回答:
(1)石灰乳参与反应的化学方程式为Ca(OH)2+SO2═CaSO3+H2O.
(2)“浸锰”反应中往往有副产物MnS2O6的生成,温度对“浸锰”反应的影响如下图,为减少MnS2O6 的生成,“浸锰”过程适宜的温度是150℃(或150℃以上).

(3)查阅下表回答②中加入一定量纯MnO2粉末的主要作用是将Fe2+氧化为Fe3+,将过量的SO2氧化除去.
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
(5)④中加入NH4HCO3后发生反应的离子方程式是Mn2++2HCO3-=MnCO3↓+CO2↑+H2O.
(6)已知MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解.请问用少量C2H5OH洗涤的原因是防止MnCO3潮湿时被空气氧化、便于在温度低于100℃干燥等.
17.用废旧黄铜(Cu、Zn合金,含少量Fe)制备胆矾晶体(CuSO4•5H2O)及副产物ZnO的流程为:
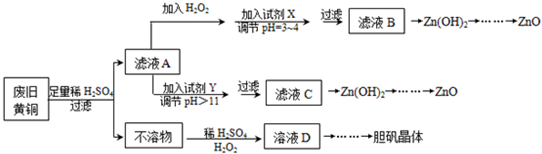
已知:①Zn及化合物性质与Al及化合物性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.
②下表为几种离子生成氢氧化物沉淀的pH(开始沉淀时金属离子浓度为1.0mol•L-1).
(1)往滤液A中加H2O2的作用是将 Fe2+氧化为Fe3+,该反应的离子方程式为2Fe2++H2O2+2H+=2Fe3++2H2O.
(2)调节pH=3~4的试剂X可以用AC:
A.ZnO B.NaOH C.Zn(OH)2 D.ZnSO4
调节pH=3~4的目的是使Fe3+转化为Fe(OH)3,达到除去Fe3+的目的.
(3)往滤液A中加的Y试剂可以是B:
A.ZnO B.NaOH C.Na2CO3D.ZnSO4
(4)由不溶物生成溶液D的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O.
(5)由溶液D制胆矾晶体包含的主要操作步骤是蒸发浓缩、冷却结晶、抽滤、晾干.
(6)测定胆矾晶体纯度(不含能与I-反应的杂质):准确称取0.5000g胆矾晶体置于锥形瓶,加适量水溶解,再加过量KI,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液19.60mL,离子反应为:
2Cu2++4I-═2CuI(白色)↓+I2,I2+2S2O32-═2I-+S4O62-
①胆矾晶体的纯度为98.00%.
②若滴定前仰视、滴定后俯视滴定管读数,所测纯度将会偏低(填“偏高”、“偏低”或“不变”).
0 153862 153870 153876 153880 153886 153888 153892 153898 153900 153906 153912 153916 153918 153922 153928 153930 153936 153940 153942 153946 153948 153952 153954 153956 153957 153958 153960 153961 153962 153964 153966 153970 153972 153976 153978 153982 153988 153990 153996 154000 154002 154006 154012 154018 154020 154026 154030 154032 154038 154042 154048 154056 203614

已知:①Zn及化合物性质与Al及化合物性质相似,pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.
②下表为几种离子生成氢氧化物沉淀的pH(开始沉淀时金属离子浓度为1.0mol•L-1).
| Fe3+ | Fe2+ | Zn2+ | |
| 开始沉淀的pH | 1.1 | 5.8 | |
| 沉淀完全的pH | 3.0 | 8.8 | 8.9 |
(2)调节pH=3~4的试剂X可以用AC:
A.ZnO B.NaOH C.Zn(OH)2 D.ZnSO4
调节pH=3~4的目的是使Fe3+转化为Fe(OH)3,达到除去Fe3+的目的.
(3)往滤液A中加的Y试剂可以是B:
A.ZnO B.NaOH C.Na2CO3D.ZnSO4
(4)由不溶物生成溶液D的化学方程式为Cu+H2O2+H2SO4=CuSO4+2H2O.
(5)由溶液D制胆矾晶体包含的主要操作步骤是蒸发浓缩、冷却结晶、抽滤、晾干.
(6)测定胆矾晶体纯度(不含能与I-反应的杂质):准确称取0.5000g胆矾晶体置于锥形瓶,加适量水溶解,再加过量KI,用0.1000mol•L-1Na2S2O3标准溶液滴定至终点,消耗Na2S2O3标准溶液19.60mL,离子反应为:
2Cu2++4I-═2CuI(白色)↓+I2,I2+2S2O32-═2I-+S4O62-
①胆矾晶体的纯度为98.00%.
②若滴定前仰视、滴定后俯视滴定管读数,所测纯度将会偏低(填“偏高”、“偏低”或“不变”).
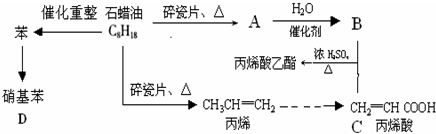
 A→B的反应类型:加成反应
A→B的反应类型:加成反应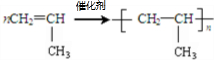 ;
;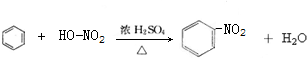 ,
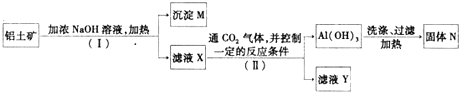
,
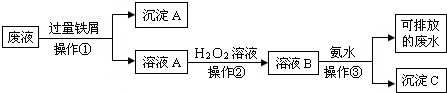
 碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.
碱式碳酸铜是一种具有广泛用途的化工产品,主要用于固体荧光粉激活剂和铜盐的制造等.