题目内容
19. 高纯MnCO3是制备高性能磁性材料的主要原料.某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):
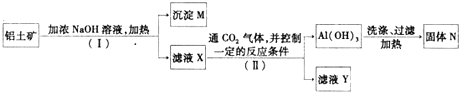
高纯MnCO3是制备高性能磁性材料的主要原料.某化学小组在实验室模拟用软锰矿(主要成分MnO2,杂质为铁及铜的化合物等)制备高纯碳酸锰,过程如下(部分操作和条件略):①缓慢向烧瓶中(见图)通入过量混合气进行“浸锰”操作,主要反应原理为:SO2+H2O=H2SO3;MnO2+H2SO3=MnSO4+H2O(铁浸出后,过量的SO2会将Fe3+还原为Fe2+)
②向“浸锰”结束后的烧瓶中加入一定量纯MnO2粉末.
③再用Na2CO3溶液调节pH为3.5左右,过滤.
④调节滤液pH为6.5~7.2,加入NH4HCO3,有无色无味的气体放出,同时有浅红色的沉淀生成,经过滤、洗涤、干燥,得到高纯碳酸锰.请回答:
(1)石灰乳参与反应的化学方程式为Ca(OH)2+SO2═CaSO3+H2O.
(2)“浸锰”反应中往往有副产物MnS2O6的生成,温度对“浸锰”反应的影响如下图,为减少MnS2O6 的生成,“浸锰”过程适宜的温度是150℃(或150℃以上).

(3)查阅下表回答②中加入一定量纯MnO2粉末的主要作用是将Fe2+氧化为Fe3+,将过量的SO2氧化除去.
| 物质 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 |
| 开始沉淀pH | 2.7 | 7.6 | 8.3 | 4.7 |
| 完全沉淀pH | 3.7 | 9.6 | 9.8 | 6.7 |
(5)④中加入NH4HCO3后发生反应的离子方程式是Mn2++2HCO3-=MnCO3↓+CO2↑+H2O.
(6)已知MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解.请问用少量C2H5OH洗涤的原因是防止MnCO3潮湿时被空气氧化、便于在温度低于100℃干燥等.
分析 (1)反应装置中石灰乳是用来吸收尾气的,实验中的尾气中含有二氧化硫,用石灰乳吸收;
(2)选择Mn2+的浸出率最大、MnS2O6的生成率最小时温度;
(3)二氧化锰有氧化性,能分别和亚铁离子、二氧化硫发生氧化还原反应,再调节溶液pH将铁离子转化为氢氧化铁沉淀除去;
(4)根据平衡移动的原理,当生成物的浓度减少时,平衡向正反应方向移动,CuS比MnS更难溶,MnS不断溶解生成更难溶的CuS;
(5)④中加入NH4HCO3后,有浅红色的沉淀生成为碳酸锰,生成的无色气体为二氧化碳;
(6)MnCO3难溶于水和乙醇,但潮湿时易被空气氧化,所以不能用水洗涤,而用乙醇洗涤,同时乙醇易挥发,所以可以在100℃以下干燥.
解答 解:(1)反应装置中石灰乳是用来吸收尾气的,实验中的尾气中含有二氧化硫,用石灰乳吸收,反应的化学方程式为Ca(OH)2+SO2═CaSO3+H2O,
故答案为:Ca(OH)2+SO2═CaSO3+H2O;
(2)当温度150℃以上时,MnS2O6的生成率几乎为0,高于30℃以上Mn2+的浸出率提高不大,“浸锰”的适宜温度是150℃(或150℃以上),
故答案为:150℃(或150℃以上);
(3)二氧化锰有氧化性,能氧化二价铁离子和二氧化硫,所以②中加入一定量纯MnO2粉末,能将Fe2+氧化为Fe3+,将过量的SO2氧化除去,再调节溶液pH将铁离子转化为氢氧化铁沉淀除去,
故答案为:将Fe2+氧化为Fe3+,将过量的SO2氧化除去;
(4)③中所得的滤液中含有Cu2+,添加过量的难溶电解质MnS,CuS比MnS更难溶,所以MnS不断溶解,MnS(S)?Mn2+(aq)+S2-(aq)、S2-(aq)+Cu2+(aq)?CuS(S)平衡右移,使Cu2+除去,
故答案为:MnS(S)?Mn2+(aq)+S2-(aq)、S2-(aq)+Cu2+(aq)?CuS(S) 生成的CuS比MnS更难溶,促进MnS不断溶解,平衡右移,使Cu2+除去;
(5)④中加入NH4HCO3后,有浅红色的沉淀生成为碳酸锰,生成的无色气体为二氧化碳,反应方程式为:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O,
故答案为:Mn2++2HCO3-=MnCO3↓+CO2↑+H2O;
(6)MnCO3难溶于水和乙醇,但潮湿时易被空气氧化,所以不能用水洗涤,而用乙醇洗涤,同时乙醇易挥发,所以可以在100℃以下干燥,
故答案为:防止MnCO3潮湿时被空气氧化、便于在温度低于100℃干燥等.
点评 本题考查物质制备实验,题目综合性,注意对题目信息的应用、控制操作条件与物质的分离提纯,侧重考查学生对知识的综合应用,难度中等.

族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
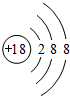
(2)用电子式表示②与④形成化合物的过程
 .
.(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)写出⑤与氢氧化钠反应的化学方程式:2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
写出⑤的氢氧化物与氢氧化钠溶液反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
| A. | Fe | B. | Cu | C. | 氯水 | D. | KSCN溶液 |
 已知:下表为25℃时某些弱酸的电离平衡常数.
已知:下表为25℃时某些弱酸的电离平衡常数.| CH3COOH | HClO | H2CO3 |
| Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.4×10-7Ka2=4.7×10-11 |
| A. | 25℃时,相同浓度的CH3COONa溶液的碱性大于NaClO溶液 | |
| B. | 向NaClO溶液中通入少量二氧化碳的离子方程式为2ClO-+CO2+H2O═2HClO+CO${\;}_{3}^{2-}$ | |
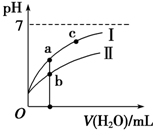
| C. | 图象 I代表CH3COOH溶液的稀释 | |
| D. | 图象中a点酸的总浓度大于b点酸的总浓度 |
(1)已知:2CO(g)+O2(g)═2CO2(g);△H=-566kJ•moL-1
2H2(g)+O2(g)═2H2O(g);△H=-483.6KJ•moL-1
H2O (g)═H2O(l);△H=-44.0KJ•moL-1
写出CO和H2O(g)作用生成CO2和H2的热化学方程式CO(g)+H2O(g)=H2(g)+CO2(g)△H=-41.2KJ•moL-1
(2)在850℃时,反应:CO(g)+H2O(g)?CO2(g)+H2(g)的K=1.
①:若升高温度到950℃时,达到平衡时K<1(填“>”、“<”或“=”).
②:850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和x mol H2,若要使上述反应开始时向正反应方向进行,则x应满足的条件是x<3.
③:在②的条件下,按下列加料方式加料,达到平衡时H2的体积分数如下:
| 加料方式(mol) | H2的体积分数 | ||||
| 物质 | CO(g) | H2O(g) | CO2(g) | H2(g) | |
| 加料一 | 1 | 3 | 0 | 0 | a% |
| 加料二 | 0 | 1.2 | 0.6 | 0.6 | b% |
(3)H2是一种理想的绿色能源,可作燃料电池.
①若该氢氧燃料电池以KOH为电解质溶液,其正极的电极反应式是O2+4e-+2H2O═4OH-
②在25℃时,以氢氧燃料电池为电源,用石墨电极电解1000mL一定浓度的CuSO4溶液.5min后电解完全,在一个石墨电极上只有1.28g Cu生成.试回答下列问题:
电解的总反应式为2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4.
电解过程中转移的电子数为0.08mol,同时生成标准状况下气体的体积为0.896L.
| A. | Mg和Zn | B. | Mg和Al | C. | Fe和Zn | D. | Cu和Fe |