题目内容
18.钛是继铁、铝后的第三金属,二氧化钛广泛应用于各类结构表面涂料、纸张涂层等,二氧化钛还可作为制备钛单质的原料.Ⅰ.用钛铁矿制取二氧化钛,(钛铁矿主要成分为FeTiO3,其中Ti元素化合价为+4价,含有Fe2O3杂质.)主要流程如下:
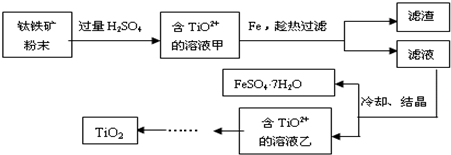
(1)Fe2O3与H2SO4反应的离子方程式Fe2O3+6H+=2Fe3++3H2O.
(2)加Fe的作用是将Fe3+还原为Fe2+.
Ⅱ.由金红石(含TiO2大于96%)为原料生产钛的流程如下:
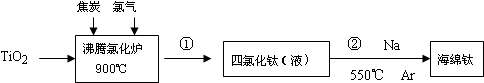
(3)反应②的方程式是TiCl4+4Na$\frac{\underline{\;550℃\;}}{氩气}$4NaCl+Ti,该反应需要在Ar气氛中进行的原因是防止高温下Na(Ti)与空气中的O2(或N2、CO2)作用.
(4)海棉钛通常需要经过真空电弧炉里熔炼提纯,也可通过碘提纯法,原理为:
Ti(s)+2I2(g)$?_{约1250℃}^{400℃}$TiI4(g)下列说法正确的是(d).
(a) 该反应的△H>0
(b) 在不同温度区域,TiI4的量保持不变
(c) 在提纯过程中,I2的量不断减少
(d) 在提纯过程中,I2的作用是将粗钛从低温区转移到高温区
Ⅲ.科学家从电解冶炼铝的工艺得到启发,找出了冶炼钛的新工艺.

(5)TiO2直接电解法生产钛是一种较先进的方法,电解质为熔融的氧化钙,原理如右图所示 该方法阴极获得钛的电极反应为TiO2+4e-=Ti+2O2-.
(6)在上述方法的基础上发明了一种更加绿色环保的技术,阳极改用金属陶瓷,并在阳极通入某种常见的还原性气体单质,则生成无污染的电极产物.通入的气体是H2.
分析 I.钛铁矿用硫酸溶解,得到溶液中含有TiO2+、Fe2+、Fe3+,加入Fe粉将Fe3+还原为Fe2+,过滤除去不溶物,滤液冷却结晶析出硫酸亚铁晶体,过滤分离,滤液中经过系列转化得到TiO2;
(1)Fe2O3与H2SO4反应生成硫酸铁与水;
(2)加入Fe粉将Fe3+还原为Fe2+;
Ⅱ.(3)在550℃时、氩气环境下,Na与四氯化钛发生置换反应;高温时,Na、Ti易与空气中的氧气等发生反应;
(4)(a)较低温度下有利于反应正向进行,高温下有利于反应逆向进行,说明正反应为放热反应;
(b) 高于400℃,钛和碘反应生成TiI4,大于1250℃TiI4分解;
(c)400℃时碘和钛反应生成四氯化钛,在1250℃四氯化钛分解生成碘和钛,I2循环利用;
(d)低温得到TiI4(g),高温下TiI4(g)分解得到Ti(s)与I2(g),在提纯过程中,I2的作用是将粗钛从低温区转移到高温区.
Ⅲ.TiO2直接电解法生产钛,发生还原反应,二氧化钛为阴极,连接电源负极,由示意图可知二氧化钛获得电子生成Ti与氧离子;石墨为阳极,阳极发生氧化反应,氧离子在阳极获得电子生成氧气,会与石墨反应生成CO等有毒气体,石墨改为某金属陶瓷电极并通入一种还原性气体,反应后的生成物没有污染,可以是生成水.
解答 解:I.钛铁矿用硫酸溶解,得到溶液中含有TiO2+、Fe2+、Fe3+,加入Fe粉将Fe3+还原为Fe2+,过滤除去不溶物,滤液冷却结晶析出硫酸亚铁晶体,过滤分离,滤液中经过系列转化得到TiO2;
(1)Fe2O3与H2SO4反应生成硫酸铁与水,反应离子方程式为:Fe2O3+6H+=2Fe3++3H2O,故答案为:Fe2O3+6H+=2Fe3++3H2O;
(2)加Fe的作用是:将Fe3+还原为Fe2+,故答案为:将Fe3+还原为Fe2+;
Ⅱ.(3)在550℃时、氩气环境下,Na与四氯化钛发生置换反应,反应方程式为:TiCl4+4Na$\frac{\underline{\;550℃\;}}{氩气}$4NaCl+Ti,高温时,Na、Ti易与空气中的氧气等发生反应,所以该反应需要在Ar气氛中进行,
故答案为:TiCl4+4Na$\frac{\underline{\;550℃\;}}{氩气}$4NaCl+Ti;防止高温下Na(Ti)与空气中的O2(或N2、CO2)作用;
(4)(a)较低温度下有利于反应正向进行,高温下有利于反应逆向进行,说明正反应为放热反应,则该反应正反应的△H<0,故错误;
(b)高于400℃,钛和碘反应生成TiI4,大于1250℃TiI4分解,故B错误;
(c)400℃时碘和钛反应生成四氯化钛,在1250℃四氯化钛分解生成碘和钛,I2循环利用,I2的量不变,故错误;
(d)在提纯过程中,高于400℃,钛和碘反应生成TiI4,大于1250℃TiI4分解,所以I2的作用是将粗钛从低温区转移到高温区,故正确;
故选:(d);
Ⅲ.(5)TiO2直接电解法生产钛,发生还原反应,二氧化钛为阴极,连接电源负极,由示意图可知二氧化钛获得电子生成Ti与氧离子,阴极电极反应式为:TiO2+4e-=Ti+2O2-,
故答案为:TiO2+4e-=Ti+2O2-;
(6)石墨为阳极,阳极发生氧化反应,氧离子在阳极获得电子生成氧气,会与石墨反应生成CO等有毒气体,石墨改为某金属陶瓷电极并通入一种还原性气体,反应后的生成物没有污染,可以是生成水,所以该气体是氢气,
故答案为:H2;
(c) 在提纯过程中,高于400℃,碘和钛反应生成四氯化钛,在1250℃四氯化钛分解生成碘和钛,所以I2的量不变,故错误;
(d) 在提纯过程中,高于400℃,碘和钛反应生成四氯化钛,在1250℃四氯化钛分解生成碘和钛,所以I2的作用是将粗钛从低温区转移到高温区,故正确;
故答案为:d;
III.(5)电解时,阴极上得电子发生还原反应,所以二氧化钛得电子生成钛和氧离子,和电源负极相连,电极反应式为TiO2+4e-=Ti+2O2-;
故答案为:TiO2+4e-=Ti+2O2-;
(6)阴极上加入的物质应该具有还原性且是气体,反应后的生成物没有污染,水没有污染,所以该气体是氢气,故答案为:H2.
点评 本题以金属的冶炼为载体,考查化学工艺流程、电解原理、化学平衡移动、信息获取等问题,有利于培养学生分析解决问题能力、信息获取与知识移运用,难度中等.

| A. | 过量氨水与氯化铝溶液反应:Al3++3OH-═Al(OH)3↓ | |
| B. | 氢氧化铝溶于稀盐酸中:H++OH-═H2O | |
| C. | 氢氧化铝溶于氢氧化钠溶液:Al(OH)3+OH-═AlO2-+2H2O | |
| D. | 过量氢氧化钠溶液与氯化铝溶液反应:Al3++3OH-═Al(OH)3↓ |
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |

存在的主要副反应有:在温度稍高的情况下会生成间二硝基苯.
有关数据列如表:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 间二硝基苯 | 89 | 301 | 1.57 | 微溶于水 |
| 浓硝酸 | 83 | 1.4 | 易溶于水 | |
| 浓硫酸 | 338 | 1.84 | 易溶于水 |
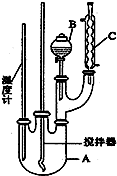
实验步骤如下:
取100mL烧杯,用20mL浓硫酸与18mL浓硝酸配制混和酸,将混合酸小心加入B中.把18mL(15.84g)苯加入A中.向室温下的苯中逐滴加入混酸,边滴边搅拌,混和均匀.在50~60℃下发生反应,直至反应结束.
将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5%NaOH溶液和水洗涤.分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210℃馏分,得到纯硝基苯18g.
回答下列问题:
(1)装置B的名称是分液漏斗.装置C的作用是冷凝回流.
(2)配制混合酸时,能否将浓硝酸加入到浓硫酸中,说明理由:不能,容易发生迸溅.
(3)为了使反应在50℃~60℃下进行,常用的方法是水浴加热.
(4)在洗涤操作中,第二次水洗的作用是洗去残留的NaOH及生成的盐.
(5)在蒸馏纯化过程中,因硝基苯的沸点高于140℃,应选用空气冷凝管,不选用直形冷凝管的原因是以免直形冷凝管通水冷却时导致温差过大而发生炸裂.
(6)本实验所得到的硝基苯产率是72%.
| A. | CH3COOH的电离程度变大 | B. | c(CH3COO-)增大 | ||
| C. | CH3COOH的Ka不变 | D. | 溶液的pH增大 |
| A. | 溶液和胶体的本质区别是否有丁达尔效应 | |
| B. | 用pH试纸测定某新制氯水的pH为4 | |
| C. | 酸性氧化物不一定都可与水反应生成酸,金属氧化物不一定是碱性氧化物 | |
| D. | 少量SO2和CO2气体分别通入BaCl2溶液中均有白色沉淀产生 |
 海南某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验.
海南某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验.