12.常用的锌锰干电池在放电时总反应可表示为:Zn+2NH4+═Zn2++2NH3+H2,则下列说法中正确的是( )
| A. | 电池工作时,电子由正极通过外电路流向负极 | |
| B. | 电池工作时,阳离子向负极移动 | |
| C. | 放电时Zn参与反应的电极为正极 | |
| D. | 外电路中每通过0.2 mol电子,锌的质量理论上减小6.5 g |
11.下列说法不正确的是( )
| A. | 反应是放热还是吸热必须看生成物和反应物所具有的总能量的相对大小 | |
| B. | 绿色植物进行光合作用时,将太阳能转化为化学能储存起来 | |
| C. | 吸热反应都要加热才能进行 | |
| D. | 物质的化学能可以在一定条件下转化为热能、电能为人类所利用 |
9.AgN03是一种重要的化学试剂,精炼铜的阳极泥中含有较多的银,可用于制备AgN03,主要工艺流程如图:

已知:AgNO3与Cu( N03)2受热易分解,分解温度如表所示.
(1)黑色固体D的化学式为CuO,①中加热温度的范围应控制在473-673K.
(2)如表为不同温度时AgNO3的溶解度
据此判断,②中从溶液Ⅱ中获得纯净的AgN03晶体的主要操作为:蒸发浓缩→过滤冷却结晶→过滤→洗涤→干燥.
(3)气体甲可以与NaOH溶液反应,产物之一为NaN02.已知常温时Ka(HN02)=4.9x10-4,常温下将0.1mol•L-1 NaOH溶液与0.2mol•L-1HN02溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(NO2-)>c(Na+)>c(H+)>c(OH-).
(4)另一种提纯AgN03溶液的方法为:向含有Cu2+的AgNO3溶液中加入某固体,充分反应后滤去蓝色沉淀即可,该固体可以为D(填选项字母).
A.NaOH B.AgCl C.FeS D.Ag2O
(5)制得的AgN03可配制为标准溶液,在中性或弱碱性溶液中,以K2Cr04为指示剂测定氯化物中Cl-的含量,主要反应为:
Ag++Cl-═AgCl↓ 2Ag++Cr042-(黄色)═Ag2Cr04↓砖红色)
已知Ksp(AgCl)=1.8×lO-10,Ksp(AgCrO4)=1.2×l0-12,则用该方法测定NaCl溶液中的c(Cl-)时,达到滴定终点时的现象为当滴入最后一滴AgNO3后有砖红色沉淀生成;实验中指示剂K2Cr04的浓度不宜过大,原因为K2CrO4溶液为黄色,浓度过大将影响滴定终点现象的判断(或K2CrO4溶液浓度过大时,有可能会在Cl-未完全沉淀时与Ag+结合,对滴定结果造成误差).

已知:AgNO3与Cu( N03)2受热易分解,分解温度如表所示.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 122 | 216 | 311 | 440 | 585 | 733 |
(2)如表为不同温度时AgNO3的溶解度
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 122 | 216 | 311 | 440 | 585 | 733 |
(3)气体甲可以与NaOH溶液反应,产物之一为NaN02.已知常温时Ka(HN02)=4.9x10-4,常温下将0.1mol•L-1 NaOH溶液与0.2mol•L-1HN02溶液等体积混合后,溶液中离子浓度由大到小的顺序为c(NO2-)>c(Na+)>c(H+)>c(OH-).
(4)另一种提纯AgN03溶液的方法为:向含有Cu2+的AgNO3溶液中加入某固体,充分反应后滤去蓝色沉淀即可,该固体可以为D(填选项字母).
A.NaOH B.AgCl C.FeS D.Ag2O
(5)制得的AgN03可配制为标准溶液,在中性或弱碱性溶液中,以K2Cr04为指示剂测定氯化物中Cl-的含量,主要反应为:
Ag++Cl-═AgCl↓ 2Ag++Cr042-(黄色)═Ag2Cr04↓砖红色)
已知Ksp(AgCl)=1.8×lO-10,Ksp(AgCrO4)=1.2×l0-12,则用该方法测定NaCl溶液中的c(Cl-)时,达到滴定终点时的现象为当滴入最后一滴AgNO3后有砖红色沉淀生成;实验中指示剂K2Cr04的浓度不宜过大,原因为K2CrO4溶液为黄色,浓度过大将影响滴定终点现象的判断(或K2CrO4溶液浓度过大时,有可能会在Cl-未完全沉淀时与Ag+结合,对滴定结果造成误差).
8.下列关于有机物的说法正确的是( )
| A. | 乙烯和苯都能与溴水反应 | |
| B. | 甲烷、乙烯和苯在工业上都可通过石油分馏得到 | |
| C. | 有机物分子中都存在碳碳单键 | |
| D. | 乙醇可以被氧化为乙酸,二者都能发生酯化反应 |
6.绿矾(FeSO4•7H2O)广泛用于工农业生产.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生成纯净绿矾的一种方法:
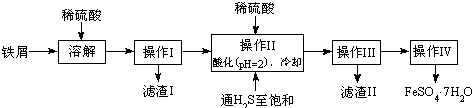
查询资料,得有关物质的数据如下表:
(1)操作II中,通入硫化氢至饱和的目的是除去Sn2+并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+沉淀;
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其洗涤的目的是洗去晶体表面的硫酸等杂质;用冰水的原因是降低晶体的溶解度,减少溶解导致FeSO4•7H2O的损耗;
(3)次氯酸盐在碱性条件下氧化硫酸亚铁可得高冷净水剂K2FeO4,离子方程式为2ClO-+Fe2++4OH-=FeO42-+2Cl-+2H2O;
(4)25℃时,将FeSO4•7H2O样品溶于水配成FeSO4溶液,该溶液中的Fe2+在空气中易被氧化成Fe3+,若向完全被氧化后的溶液中滴加NaOH溶液,当滴至溶液的pH=4时,溶液中的c(Fe3+)=4.0×10-8mol/L.[已知该温度下,Fe(OH)3的Ksp=4.0×10-38]
(5)将8.34gFeSO4•7H2O样品隔绝空气加热脱水,其重曲线(样品质量随温度变化的曲线)如图所示: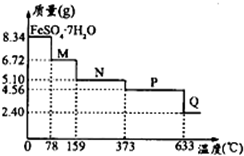
①在100℃时M的化学式为FeSO4•4H2O;
②FeSO4•7H2O晶体中有3种不同结合力的水分子.

查询资料,得有关物质的数据如下表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其洗涤的目的是洗去晶体表面的硫酸等杂质;用冰水的原因是降低晶体的溶解度,减少溶解导致FeSO4•7H2O的损耗;
(3)次氯酸盐在碱性条件下氧化硫酸亚铁可得高冷净水剂K2FeO4,离子方程式为2ClO-+Fe2++4OH-=FeO42-+2Cl-+2H2O;
(4)25℃时,将FeSO4•7H2O样品溶于水配成FeSO4溶液,该溶液中的Fe2+在空气中易被氧化成Fe3+,若向完全被氧化后的溶液中滴加NaOH溶液,当滴至溶液的pH=4时,溶液中的c(Fe3+)=4.0×10-8mol/L.[已知该温度下,Fe(OH)3的Ksp=4.0×10-38]
(5)将8.34gFeSO4•7H2O样品隔绝空气加热脱水,其重曲线(样品质量随温度变化的曲线)如图所示:

①在100℃时M的化学式为FeSO4•4H2O;
②FeSO4•7H2O晶体中有3种不同结合力的水分子.
4.下列离子检验的方法正确的是( )
0 153839 153847 153853 153857 153863 153865 153869 153875 153877 153883 153889 153893 153895 153899 153905 153907 153913 153917 153919 153923 153925 153929 153931 153933 153934 153935 153937 153938 153939 153941 153943 153947 153949 153953 153955 153959 153965 153967 153973 153977 153979 153983 153989 153995 153997 154003 154007 154009 154015 154019 154025 154033 203614
| A. | 某溶液中滴加AgNO3溶液有白色沉淀,说明原溶液中有Cl- | |
| B. | 某溶液中先滴加足量盐酸无规象,再滴加BaCl2溶液有白色沉淀.则原溶液中有SO42- | |
| C. | 某无色溶液滴入酚酞试液显红色,该溶液一定是含有大量的H+ | |
| D. | 某溶液中滴加盐酸生成能使澄清石灰水变浑浊的无色气体,说明原溶液中有CO32- |


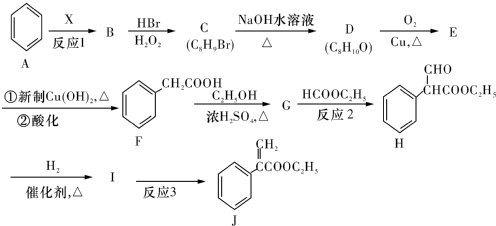
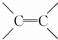 (或碳碳双键).
(或碳碳双键). .
.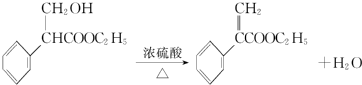 .
.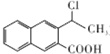 为起始原料制备
为起始原料制备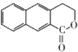 的合成路线
的合成路线 .
.