��Ŀ����
3������������J����һ���������Ƶĸ���ҩ���ϳ�·�����£�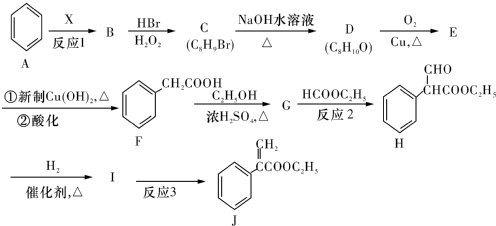
�Իش��������⣺
��1����B����Է�������С��118�������������������Ϊ7.69%���ҷ�Ӧ1Ϊ�ӳɷ�Ӧ����X������Ϊ��Ȳ��B���еĹ�������
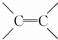 ����̼̼˫������
����̼̼˫��������2��G��H �ķ�Ӧ����Ϊȡ����Ӧ��
��3��C�Ľṹ��ʽΪ
 ��
����4����Ӧ3�Ļ�ѧ����ʽΪ
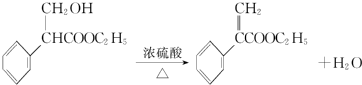 ��
����5��������I�ж���ͬ���칹�壬ͬʱ�������������Ľṹ��6�֣�
���ܷ���ˮ�ⷴӦ��������Ӧ��������FeC13������ɫ��Ӧ���۱��������ĸ�ȡ�������ұ�����һ±����ֻ��һ��
��6�����յ��������ĺϳ�·�ߣ����һ����
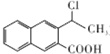 Ϊ��ʼԭ���Ʊ�
Ϊ��ʼԭ���Ʊ�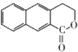 �ĺϳ�·��
�ĺϳ�·�� ��
��
���� ���ݺϳ���·��֪��E������Cu��OH ��2���������·�Ӧ���ữ���F��E�к���ȩ������E�Ľṹ��ʽΪ�� ��D����������E����D�Ľṹ��ʽΪ��
��D����������E����D�Ľṹ��ʽΪ�� ��Cˮ������D����C�Ľṹ��ʽΪ��
��Cˮ������D����C�Ľṹ��ʽΪ��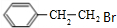 ��B������Ӧ����C��BΪ��������C����ʽ֪��B�ṹ��ʽΪ
��B������Ӧ����C��BΪ��������C����ʽ֪��B�ṹ��ʽΪ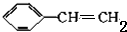 ����Ӧ1Ϊ�ӳɷ�Ӧ����XΪHC��CH��
����Ӧ1Ϊ�ӳɷ�Ӧ����XΪHC��CH��
F��CH3CH2OH��Ũ������������£�����������Ӧ���ɵ�G����G�Ľṹ��ʽΪ ��H��H2�ӳɣ�ȩ��ת��Ϊ�ǻ�����I�Ľṹ��ʽΪ��
��H��H2�ӳɣ�ȩ��ת��Ϊ�ǻ�����I�Ľṹ��ʽΪ�� ��
��
��6������ͨ����ȥ��Ӧ�õ�̼̼˫������H2O2��������HBr�ӳɣ�Br�ڶ˵��Cԭ���ϣ�ˮ�ⷴӦ����-OH��Ȼ����������Ӧ�����ղ��
�ݴ˷������
��� �⣺���ݺϳ���·��֪��E������Cu��OH ��2���������·�Ӧ���ữ���F��E�к���ȩ������E�Ľṹ��ʽΪ�� ��D����������E����D�Ľṹ��ʽΪ��
��D����������E����D�Ľṹ��ʽΪ�� ��Cˮ������D����C�Ľṹ��ʽΪ��
��Cˮ������D����C�Ľṹ��ʽΪ��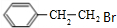 ��B������Ӧ����C��BΪ��������C����ʽ֪��B�ṹ��ʽΪ
��B������Ӧ����C��BΪ��������C����ʽ֪��B�ṹ��ʽΪ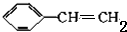 ����Ӧ1Ϊ�ӳɷ�Ӧ����XΪHC��CH��
����Ӧ1Ϊ�ӳɷ�Ӧ����XΪHC��CH��
F��CH3CH2OH��Ũ������������£�����������Ӧ���ɵ�G����G�Ľṹ��ʽΪ ��H��H2�ӳɣ�ȩ��ת��Ϊ�ǻ�����I�Ľṹ��ʽΪ��
��H��H2�ӳɣ�ȩ��ת��Ϊ�ǻ�����I�Ľṹ��ʽΪ�� ��
��
��1��ͨ�����Ϸ���֪��XΪ��Ȳ��BΪ����ϩ��������Ϊ ����̼̼˫������
����̼̼˫������
�ʴ�Ϊ����Ȳ�� ����̼̼˫������
����̼̼˫������
��2��G�ͼ�����������ȡ����Ӧ����H����Ӧ������ȡ����Ӧ���ʴ�Ϊ��ȡ����Ӧ��
��3��ͨ�����Ϸ���֪��C�ṹ��ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��4����Ӧ3�Ļ�ѧ����ʽΪ ���ʴ�Ϊ��
���ʴ�Ϊ�� ��
��
��5��I�� ���ж���ͬ���칹�壮ͬʱ����������������FeCl3��Һ������ɫ��Ӧ�����з��ǻ����ܷ���ˮ�ⷴӦ��������Ӧ�����м����γɵ������������������ĸ�ȡ�������ұ�����һ�ȴ���ֻ��1�֣�����������ͬ���칹���У�
���ж���ͬ���칹�壮ͬʱ����������������FeCl3��Һ������ɫ��Ӧ�����з��ǻ����ܷ���ˮ�ⷴӦ��������Ӧ�����м����γɵ������������������ĸ�ȡ�������ұ�����һ�ȴ���ֻ��1�֣�����������ͬ���칹���У� ��
�� ��
�� ��
�� ��
�� ��
�� ���ܹ���6�֣�
���ܹ���6�֣�
�ʴ�Ϊ��6��
��6������ͨ����ȥ��Ӧ�õ�̼̼˫������H2O2��������HBr�ӳɣ�Br�ڶ˵��Cԭ���ϣ�ˮ�ⷴӦ����-OH��Ȼ����������Ӧ�����ղ�����Ժϳ�·��ͼΪ�� ��
��
�ʴ�Ϊ�� ��
��
���� ���⿼���л��ϳɼ��ƶϣ�Ϊ��Ƶ���㣬�漰�л���Ӧ���͡�ͬ���칹����д���л���Ӧ����ʽ��֪ʶ����ȷ�����ż������ʹ�ϵ�ǽⱾ��ؼ�����5����ͬ���칹�����дΪ�״��㡢�ѵ㣬��Ŀ�Ѷ��еȣ�

| A�� | 100mL��Ͳ | B�� | ������ | C�� | ������ƽ | D�� | 50mL����ƿ | ||||
| E�� | 10mL��Ͳ | F�� | ��ͷ�ι� | G�� | 50mL�ձ� | H�� | 100mL����ƿ |
| A�� | ��ij��Һ�е����������ᣬ��۲쵽��ɫ��ζ���������������ʹ����ʯ��ˮ����ǣ���֤����Һ�бض���CO32- | |
| B�� | ��ij��ɫ��Һ�м���BaCl2��Һ���а�ɫ�������֣��ټ���ϡ���ᣬ��������ʧ����֤����Һһ������SO42- | |
| C�� | ��ij��ɫ��Һ�м�������ϡ����������Һ����ʪ�����ɫʯ����ֽ�����Թܿڣ�����ֽ��죬��˵������Һ����NH4+ | |
| D�� | ������ɫ���ܲ����ܹ��۲쵽��ɫ���棬��һ���м�Ԫ�أ�һ����������Ԫ�� |
| A�� | ��ϩ�ͱ���������ˮ��Ӧ | |
| B�� | ���顢��ϩ�ͱ��ڹ�ҵ�϶���ͨ��ʯ�ͷ���õ� | |
| C�� | �л�������ж�����̼̼���� | |
| D�� | �Ҵ����Ա�����Ϊ���ᣬ���߶��ܷ���������Ӧ |
| A�� | ������ĵ��볣����Ki1��H2CO3����Ki��HX����Ki��HY����Ki2��H2CO3�� | |
| B�� | NaX��Һ��ͨ������CO2�������Ũ�ȣ�c��HCO3-����c��CO32-����c��X-�� | |
| C�� | ͬŨ����Һ�ļ��ԣ�NaX��Na2CO3��NaY��NaHCO3 | |
| D�� | ���H+��������Y-��CO32-��X-��HCO3- |
| A�� | ��������ˮ��Cl2+H2O�TH++Cl-+HClO | |
| B�� | ��ϡHNO3�еμ�Na2SO3��Һ��SO32-+2H+�TSO2��+H2O | |
| C�� | ������Һ��KIO3��KI��Ӧ����I2��IO3-+5I-+6H+�T3I2+3H2O | |
| D�� | ��Na2SiO3��Һ��ͨ�����SO2��SiO32-+SO2+H2O�TH2SiO3��+SO32- |