题目内容
11.下列说法不正确的是( )| A. | 反应是放热还是吸热必须看生成物和反应物所具有的总能量的相对大小 | |
| B. | 绿色植物进行光合作用时,将太阳能转化为化学能储存起来 | |
| C. | 吸热反应都要加热才能进行 | |
| D. | 物质的化学能可以在一定条件下转化为热能、电能为人类所利用 |
分析 A.化学反应的能量变化主要表现为放热或吸热,反应是放热还是吸热主要取决于反应物和生成物所具有的总能量的相对大小;
B.植物的光合作用就是太阳能转化为化学能;
C.吸热反应与反应的条件无关;
D.化学能可以通过燃烧、原电池原理转化为热能、光能、电能等.
解答 解:A.化学反应的能量变化主要表现为放热或吸热,反应是放热还是吸热主要取决于反应物和生成物所具有的总能量的相对大小,反应物的总能量大于生成物的总能量,则反应放热,反之吸热,故A正确;
B.植物的光合作用就是太阳能转化为化学能储存起来,故B正确;
C.氢氧化钡与氯化铵的反应吸热,常温下就能发生,故C错误;
D.化学能可以通过燃烧、原电池原理转化为热能、光能、电能,故D正确;
故选C.
点评 本题考查了化学反应中的能量变化,为高频考点,注意一个反应是吸热反应还是放热反应与反应的条件无关.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案
相关题目
2.下列性质的比较中,不正确的是( )
| A. | 稳定性:Na2CO3>NaHCO3 | B. | 熔点:生铁>纯铁 | ||
| C. | 酸性:H2CO3>HClO | D. | 氧化性:Fe3+>Cu2+ |
19.氯化硼的熔点为-107℃、沸点为12.5℃,在氯化硼分子中,氯-硼-氯键角为120°,它可以水解,水解产物之一是氯化氢,下列对氯化硼的叙述中正确的是( )
| A. | 氯化硼是原子晶体 | |
| B. | 熔化时,氯化硼能导电 | |
| C. | 硼原子以sp3杂化 | |
| D. | 水解方程式:BCl3+3H2O═H3BO3+3HCl |
6.绿矾(FeSO4•7H2O)广泛用于工农业生产.下面是以市售铁屑(含少量锡、氧化铁等杂质)为原料生成纯净绿矾的一种方法:
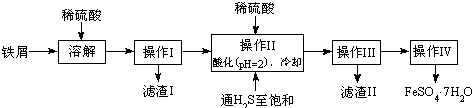
查询资料,得有关物质的数据如下表:
(1)操作II中,通入硫化氢至饱和的目的是除去Sn2+并防止Fe2+被氧化;在溶液中用硫酸酸化至pH=2的目的是防止Fe2+沉淀;
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其洗涤的目的是洗去晶体表面的硫酸等杂质;用冰水的原因是降低晶体的溶解度,减少溶解导致FeSO4•7H2O的损耗;
(3)次氯酸盐在碱性条件下氧化硫酸亚铁可得高冷净水剂K2FeO4,离子方程式为2ClO-+Fe2++4OH-=FeO42-+2Cl-+2H2O;
(4)25℃时,将FeSO4•7H2O样品溶于水配成FeSO4溶液,该溶液中的Fe2+在空气中易被氧化成Fe3+,若向完全被氧化后的溶液中滴加NaOH溶液,当滴至溶液的pH=4时,溶液中的c(Fe3+)=4.0×10-8mol/L.[已知该温度下,Fe(OH)3的Ksp=4.0×10-38]
(5)将8.34gFeSO4•7H2O样品隔绝空气加热脱水,其重曲线(样品质量随温度变化的曲线)如图所示: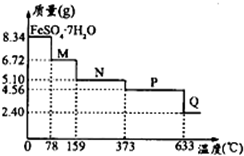
①在100℃时M的化学式为FeSO4•4H2O;
②FeSO4•7H2O晶体中有3种不同结合力的水分子.

查询资料,得有关物质的数据如下表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(2)操作IV得到的绿矾晶体用少量冰水洗涤,其洗涤的目的是洗去晶体表面的硫酸等杂质;用冰水的原因是降低晶体的溶解度,减少溶解导致FeSO4•7H2O的损耗;
(3)次氯酸盐在碱性条件下氧化硫酸亚铁可得高冷净水剂K2FeO4,离子方程式为2ClO-+Fe2++4OH-=FeO42-+2Cl-+2H2O;
(4)25℃时,将FeSO4•7H2O样品溶于水配成FeSO4溶液,该溶液中的Fe2+在空气中易被氧化成Fe3+,若向完全被氧化后的溶液中滴加NaOH溶液,当滴至溶液的pH=4时,溶液中的c(Fe3+)=4.0×10-8mol/L.[已知该温度下,Fe(OH)3的Ksp=4.0×10-38]
(5)将8.34gFeSO4•7H2O样品隔绝空气加热脱水,其重曲线(样品质量随温度变化的曲线)如图所示:

①在100℃时M的化学式为FeSO4•4H2O;
②FeSO4•7H2O晶体中有3种不同结合力的水分子.
16.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4 LH2O含有的分子数为NA | |
| B. | 1molAl3+离子含有的核外电子数为3NA | |
| C. | 3mol Fe在高温下与足量的水蒸汽反应转移的电子数为8NA | |
| D. | 1molNa2O2与足量的水反应失去电子数为2NA |
3.把500mL含BaCl2和KCl的混合溶液分成两等份,向其中一份中加入含a mol硫酸钠的溶液,恰好使钡离子完全沉淀;向另一份中加入含b mol硝酸银的溶液,恰好使氯离子完全沉淀.则该混合溶液中钾离子浓度为( )
| A. | 0.25(b-2a)mol/L | B. | 4(2a-b)mol/L | C. | 2(b-2a)mol/L | D. | 4(b-2a)mol/L |
20.工业制硫酸中的一步重要反应是2SO2+O2$?_{加热}^{催化剂}$2SO3,这是一个正反应放热的可逆反应.下列说法正确的是( )
| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 向该体系中充入18O2,一段时间后18O只存在于SO3中 | |
| C. | 生成物的总能量大于反应物的总能量 | |
| D. | 将该反应设计成原电池,放出的热量不变 |
1.鉴别Cl-、Br-、I-三种离子,宜选用的试剂是( )
| A. | 溴水和淀粉溶液 | B. | AgNO3溶液和稀硝酸 | ||
| C. | CCl4溶液 | D. | 氯水和碘化钾淀粉溶液 |
 铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题:
铁和铜都是日常生活中常见的金属,有着广泛的用途.请回答下列问题: