3.当光束通过下列分散系时,可观察到丁达尔效应的是( )
| A. | 乙醇溶液 | B. | 氨化钠溶液 | C. | 盐酸 | D. | 氢氧化铁胶体 |
2.化学概念在逻辑上存在如图所示关系. 对下列概念的说法正确的是( )

| A. | 氧化反应与化合反应属于并列关系 | B. | 单质与化合物属于交叉关系 | ||
| C. | 化合物与氧化物属于包含关系 | D. | 纯净物与混合物属于包含关系 |
1.下列叙述正确的是( )
| A. | 合金中至少含有两种金属 | |
| B. | 漂白粉能在空气中长期存放 | |
| C. | 工艺师利用氢氟酸刻蚀石英制作艺术品 | |
| D. | NaOH溶液保存在配有磨口玻璃塞的细口试剂瓶中 |
20.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 17g NH3所含的电子数是 10NA | |
| B. | 常温常压下,22.4L氧气含氧原子数为2NA | |
| C. | 5.6g铁粉与足量Cl2反应,失去的电子数为0.2NA | |
| D. | 2.3g金属钠全部变成钠离子时失去的电子数是0.2NA |
19.下列措施符合安全要求的是( )
| A. | 金属钠着火时,立即用沾水的毛巾覆盖 | |
| B. | 将含有硫酸的废液倒人水池,用大量水冲人下水道 | |
| C. | 锌和稀硫酸反应生成的氢气可直接点燃,观察火焰的颜色 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 |
18.下列物质属于纯净物的是( )
| A. | 水泥 | B. | 不锈钢 | C. | 普 通玻璃 | D. | 液氯 |
17.下列物质属于非电解质的是( )
| A. | 硫酸 | B. | 氨水 | C. | 酒精 | D. | 铜 |
14.废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如图:
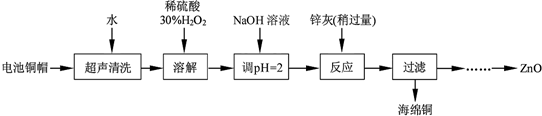
(1)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2;I2+2S2O32-═2I-+S4O62-
①Na2S2O3标准溶液应装在碱式(填酸式或碱式)滴定管内.
②滴定选用的指示剂为淀粉溶液,滴定终点观察到的现象为滴加最后一滴,颜色由蓝色变成无色,且半分钟内不变.
③若滴定前溶液中H2O2没有除尽,所测定的Cu2+的含量将会偏高(填“偏高”“偏低”“不变”).
(2)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀pH范围(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
实验中可选用的试剂:30% H2O2、1.0mol•L-1HNO3、1.0mol•L-1 NaOH.
由除去铜的滤液制备ZnO的实验步骤依次为:
①加H2O2,氧化Fe2+;
②加氢氧化钠溶液,控制PH在4左右;
③过滤;
④加氢氧化钠溶液,控制PH在8.9-11之间;
⑤过滤、洗涤、干燥
⑥900℃煅烧.
0 153554 153562 153568 153572 153578 153580 153584 153590 153592 153598 153604 153608 153610 153614 153620 153622 153628 153632 153634 153638 153640 153644 153646 153648 153649 153650 153652 153653 153654 153656 153658 153662 153664 153668 153670 153674 153680 153682 153688 153692 153694 153698 153704 153710 153712 153718 153722 153724 153730 153734 153740 153748 203614

(1)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2;I2+2S2O32-═2I-+S4O62-
①Na2S2O3标准溶液应装在碱式(填酸式或碱式)滴定管内.
②滴定选用的指示剂为淀粉溶液,滴定终点观察到的现象为滴加最后一滴,颜色由蓝色变成无色,且半分钟内不变.
③若滴定前溶液中H2O2没有除尽,所测定的Cu2+的含量将会偏高(填“偏高”“偏低”“不变”).
(2)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀pH范围(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
实验中可选用的试剂:30% H2O2、1.0mol•L-1HNO3、1.0mol•L-1 NaOH.
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
①加H2O2,氧化Fe2+;
②加氢氧化钠溶液,控制PH在4左右;
③过滤;
④加氢氧化钠溶液,控制PH在8.9-11之间;
⑤过滤、洗涤、干燥
⑥900℃煅烧.




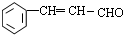 .
.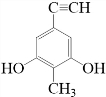 等.(任写一种)
等.(任写一种) )是一种高效麻醉剂,写出以
)是一种高效麻醉剂,写出以 、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选).合成路线流程图如下:
、CH3CHO、NH(CH3)2为原料制备呋喃丙胺的合成路线流程图(无机试剂自选).合成路线流程图如下: .
.