题目内容
14.废弃物的综合利用既有利于节约资源,又有利于保护环境.实验室利用废弃旧电池的铜帽(Zn、Cu总含量约为99%)回收铜并制备ZnO的部分实验过程如图: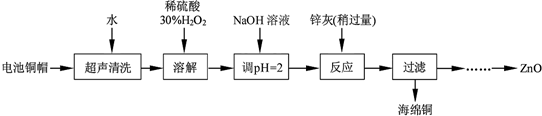
(1)为确定加入锌灰(主要成分为Zn、ZnO,杂质为铁及其氧化物)含量,实验中需测定除去H2O2后溶液中Cu2+的含量.实验操作为:准确量取一定体积的含有Cu2+的溶液于带塞锥形瓶中,加适量水稀释,调节pH=3~4,加入过量KI,用Na2S2O3标准溶液滴定至终点.上述过程中的离子方程式如下:2Cu2++4I-═2CuI(白色)↓+I2;I2+2S2O32-═2I-+S4O62-
①Na2S2O3标准溶液应装在碱式(填酸式或碱式)滴定管内.
②滴定选用的指示剂为淀粉溶液,滴定终点观察到的现象为滴加最后一滴,颜色由蓝色变成无色,且半分钟内不变.
③若滴定前溶液中H2O2没有除尽,所测定的Cu2+的含量将会偏高(填“偏高”“偏低”“不变”).
(2)已知pH>11时Zn(OH)2能溶于NaOH溶液生成[Zn(OH)4]2-.下表列出了几种离子生成氢氧化物沉淀pH范围(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
实验中可选用的试剂:30% H2O2、1.0mol•L-1HNO3、1.0mol•L-1 NaOH.
| 开始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
①加H2O2,氧化Fe2+;
②加氢氧化钠溶液,控制PH在4左右;
③过滤;
④加氢氧化钠溶液,控制PH在8.9-11之间;
⑤过滤、洗涤、干燥
⑥900℃煅烧.
分析 废弃旧电池的铜帽加水超声洗涤去除表面的可溶性杂质,然后加入稀硫酸和双氧水,双氧水具有强氧化性,能在酸性条件下氧化铜生成铜盐,加入氢氧化钠降低酸性,然后加入足量的锌灰,由于锌的活泼性强于铜,故能把铜从其盐溶液中置换出来,剩余锌的化合物制备ZnO,
(1)①Na2S2O3标准溶液因为水解呈碱性,所以要放在碱式滴定管中;
②根据淀粉与碘单质作用变蓝解答;
③若滴定前溶液中的H2O2没有除尽,则加入碘离子后双氧水氧化碘离子产生的碘单质,会导致Na2S2O3标准溶液消耗偏大,据此分析;
(3)滴加H2O2溶液,使Fe2+转化完全为Fe3+,滴加NaOH溶液,形成氢氧化铁沉淀,除杂后形成氢氧化锌沉淀,过滤、洗涤、干燥900℃煅烧制得氧化锌.
解答 解:(1)①Na2S2O3标准溶液因为水解呈碱性,所以要放在碱式滴定管中,
故答案为:碱式;
②淀粉溶液为指示剂,当最后一滴Na2S2O3溶液滴入时,溶液蓝色褪去,半分钟颜色不变,说明滴定到达终点,
故答案为:淀粉溶液;滴加最后一滴,颜色由蓝色变成无色,且半分钟内不变;
③若滴定前溶液中的H2O2没有除尽,则加入碘离子后双氧水氧化碘离子产生的碘单质,会导致Na2S2O3标准溶液消耗偏大,则所测定c (Cu2+)将会偏高,
故答案为:偏高;
(3)根据表中阳离子沉淀的PH可知,由除去铜的滤液制备ZnO的实验步骤依次为:①向滤液中加入30%H2O2,使其充分反应,目的使Fe2+转化完全为Fe3+,②加氢氧化钠溶液,控制PH在4左右,使Fe3+沉淀完全,③过滤,向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全,⑤过滤、洗涤、干燥
⑥900℃煅烧,制得氧化锌,
故答案为:加H2O2,氧化Fe2+; 加氢氧化钠溶液,控制PH在4左右;加氢氧化钠溶液,控制PH在8.9-11之间.
点评 本题主要考查实验室废弃旧电池的铜帽回收铜和制备ZnO,考查学生对综合实验处理能力,注意实验方案的设计原理和步骤是解答的关键,平时注意打好扎实的基础知识和灵活应用知识解决问题的能力培养,题目难度中等.

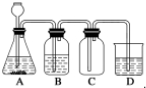
| A. | A 中可用分液漏斗代替长颈漏斗 | |
| B. | A 中缺少加热装置 | |
| C. | B 中盛放的NaOH 溶液可以净化Cl2 | |
| D. | D 中盛放的NaOH 溶液可以吸收尾气 |
| A. | 金属钠着火时,立即用沾水的毛巾覆盖 | |
| B. | 将含有硫酸的废液倒人水池,用大量水冲人下水道 | |
| C. | 锌和稀硫酸反应生成的氢气可直接点燃,观察火焰的颜色 | |
| D. | 大量氯气泄漏时,迅速离开现场并尽量往高处去 |
| A. | 溶液因不带电而稳定,胶体因带电而不稳定 | |
| B. | 定容时,因不慎使液面高于容量瓶的刻度线,需重新配制 | |
| C. | 用酒精可以从碘水中萃取碘 | |
| D. | 焰色反应是化学变化 |
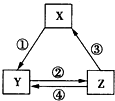 下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )
下表中各组物质之间通过一步反应不可能实现如图所示转化关系的是( )| 选项 | X | Y | Z |
| A | Mg | MgO | MgCl2 |
| B | Fe | FeCl3 | FeCl2 |
| C | Na2CO3 | NaOH | NaHCO3 |
| D | Cl2 | Ca(ClO)2 | HClO |
| A. | A | B. | B | C. | C | D. | D |