9.X、Y、Z、W、R均为第3周期主族元素,且原子序数依次增大.X、Y、W的最高价氧化物对应水化物两两之间都能发生反应,Z的单质常用作半导体.下列说法错误的是( )
| A. | X的两种氧化物中阴阳个数比均为1:2 | |
| B. | Y的氧化物熔点高,常用作耐高温材料 | |
| C. | Z的氧化物属于酸性氧化物,不能与任何酸反应 | |
| D. | R的同主族氢化物稳定性从上往下依次减弱 |
5.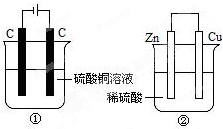 如图两个装置中,液体体积均为200ml,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mole-,若不考虑溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200ml,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mole-,若不考虑溶液体积的变化,下列叙述正确的是( )
 如图两个装置中,液体体积均为200ml,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mole-,若不考虑溶液体积的变化,下列叙述正确的是( )
如图两个装置中,液体体积均为200ml,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上都通过了0.02mole-,若不考虑溶液体积的变化,下列叙述正确的是( )| A. | 产生气体体积①=② | |
| B. | 溶液的pH变化:①减小②增大 | |
| C. | 电极上析出固体质量①<② | |
| D. | 电极反应式:①中阳极:Cu2++2e-═Cu②中负极Zn-2e-═Zn2+ |
4.在硫酸工业里,焙烧硫铁矿(FeS2)制取SO2的反应为4FeS2+11O2═2Fe2O3+8SO2.下列有关说法不正确的是( )
| A. | FeS2作还原剂,铁元素被还原 | |
| B. | Fe2O3和SO2都既是氧化产物又是还原产物 | |
| C. | 每生成1 mol Fe2O3,有4mol硫被氧化 | |
| D. | 每1 mol硫被氧化,转移电子5.5mol |
3.下列叙述正确的是( )
| A. | 同温同压下,两种气体的体积之比等于摩尔质量之比 | |
| B. | 同温同压下,两种气体的物质的量之比等于密度之比 | |
| C. | 同温同压下,两种气体的摩尔质量之比等于密度之比 | |
| D. | 同温同容下,两种气体的质量之比等于压强之比 |
2.甲、乙、丙、丁四种化合物在常温下均成气态,且均由两种相同的短周期元素组成,它们的分子中所含电子数如下表,下列关于四种物质的推断正确的是( )
| 分子代号 | 甲 | 乙 | 丙 | 丁 |
| 电子数 | 10 | 16 | 18 | 26 |
| A. | 四种气体中至少有两种气体分子互为同分异构体 | |
| B. | 四种气体通入溴的四氯化碳溶液中,都能使其褪色 | |
| C. | 气体乙的分子内所有的原子在同一平面上 | |
| D. | 鉴别丙和丁两种气体,可以用高锰酸钾酸性溶液 |
20.观察下列几个装置示意图,有关叙述不正确的是( )

0 153517 153525 153531 153535 153541 153543 153547 153553 153555 153561 153567 153571 153573 153577 153583 153585 153591 153595 153597 153601 153603 153607 153609 153611 153612 153613 153615 153616 153617 153619 153621 153625 153627 153631 153633 153637 153643 153645 153651 153655 153657 153661 153667 153673 153675 153681 153685 153687 153693 153697 153703 153711 203614

| A. | 装置①中阴极上析出红色固体 | |
| B. | 装置②的待镀铁制品应与电源负极相连 | |
| C. | 装置③中a为负极,发生的电极反应式为H2+2OH-+2e-═2H2O | |
| D. | 装置④中在阴极可以得到氢气和氢氧化钠,离子交换膜可选用阳离子交换膜 |
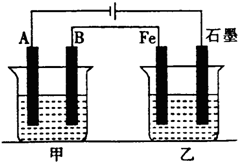 如图所示,甲、乙为相互串联的两电解池,甲池利用电解原理在铁上镀银,一段时间后,甲池阴极增重43.2g,乙中盛放足量的CuSO4溶液,请回答:
如图所示,甲、乙为相互串联的两电解池,甲池利用电解原理在铁上镀银,一段时间后,甲池阴极增重43.2g,乙中盛放足量的CuSO4溶液,请回答: 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和l00g 10.00%的K2SO4溶液.电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和l00g 10.00%的K2SO4溶液.电极均为石墨电极.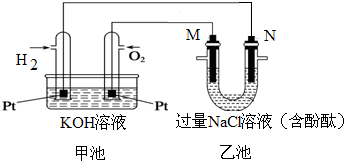 如图所示是氢氧燃料电池工作时的装置,乙池中的两个电极均是石墨电极,请回答下列问题:
如图所示是氢氧燃料电池工作时的装置,乙池中的两个电极均是石墨电极,请回答下列问题: