4.X,Y,Z为原子序数依次增大的短周期元素,且最外层电子数之和为13,X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子最外层电子数的2倍.下列说法正确的是( )
| A. | 原子半径:Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>X>Y | |
| C. | 工业上可通过电解Y的盐溶液来制备Y的单质 | |
| D. | 氧元素分别与X、Y、Z形成的化合物都不止一种 |
19.在同温同压下,1mol F2和1mol I2具有相同的( )
| A. | 体积 | B. | 原子数 | C. | 质量 | D. | 质子数. |
16.下列微粒的基态电子排布式一定错误的是( )
| A. | A原子:1s22s22p63s23p63d10 | B. | B2-:1s22s22p6 | ||
| C. | C2+:1s22s22p6 | D. | D原子:1s22s22p6 |
15.某种硬铝合金是由 Al、Cu、Mg三种金属组成,主要应用于耐热可焊的结构件及锻件.某研究小组欲探究该合金的性质并测定合金中铝的质量分数:
(1)甲同学预测:该合金与10mol/L硝酸反应时有NO2气体生成,可能还有NO生成.
查阅资料:常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在.设计如下装置进行实验.按图连接装置并检验气密性后,称取5g 合金放于圆底烧瓶中,并滴加10mol/L硝酸.
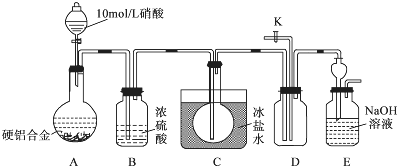
①合金中Cu与稀硝酸反应的离子方程式是3Cu+2NO3-+8H+=Cu2++2NO↑+4H2O.
②C装置的目的是将生成的NO2冷凝为N2O4,与NO分离,排除干扰.
③能证明有NO生成的实验操作与现象是打开活塞K,鼓入空气,若D中的气体由无色变为红棕色,证明有NO生成.
④实验进行至A中固体全部溶解后,未检验到有NO生成,甲同学认为硬铝合金与10mol/L硝酸反应时没有NO生成.乙同学认为不能确定是否生成了NO,需补充操作才能证明,该操作是在加入HNO3前,通入N2,除尽装置中的空气.
(2)为测定合金中铝的质量分数,丙同学查阅资料:
部分金属离子生成氢氧化物沉淀的pH
pH>7.8时,Al(OH)3开始溶解,pH>10.8时沉淀完全溶解.
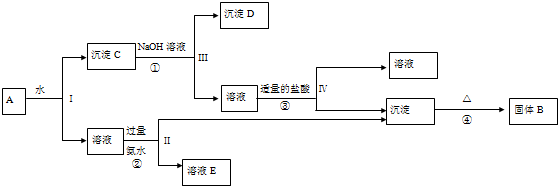
设计如下方案并进行实验:

①调节pH时,应控制pH的范围是pH≥12.4.
②选用NaOH溶液调节pH,得到溶液B的离子方程式是Al3++4OH-=AlO2-+2H2O.
③Al(OH)3经过滤、洗涤、灼烧至恒重后称量,质量为8.5g,则该合金中铝的质量分数是90%.
0 153512 153520 153526 153530 153536 153538 153542 153548 153550 153556 153562 153566 153568 153572 153578 153580 153586 153590 153592 153596 153598 153602 153604 153606 153607 153608 153610 153611 153612 153614 153616 153620 153622 153626 153628 153632 153638 153640 153646 153650 153652 153656 153662 153668 153670 153676 153680 153682 153688 153692 153698 153706 203614
(1)甲同学预测:该合金与10mol/L硝酸反应时有NO2气体生成,可能还有NO生成.
查阅资料:常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在.设计如下装置进行实验.按图连接装置并检验气密性后,称取5g 合金放于圆底烧瓶中,并滴加10mol/L硝酸.

①合金中Cu与稀硝酸反应的离子方程式是3Cu+2NO3-+8H+=Cu2++2NO↑+4H2O.
②C装置的目的是将生成的NO2冷凝为N2O4,与NO分离,排除干扰.
③能证明有NO生成的实验操作与现象是打开活塞K,鼓入空气,若D中的气体由无色变为红棕色,证明有NO生成.
④实验进行至A中固体全部溶解后,未检验到有NO生成,甲同学认为硬铝合金与10mol/L硝酸反应时没有NO生成.乙同学认为不能确定是否生成了NO,需补充操作才能证明,该操作是在加入HNO3前,通入N2,除尽装置中的空气.
(2)为测定合金中铝的质量分数,丙同学查阅资料:
部分金属离子生成氢氧化物沉淀的pH
| 金属离子 | 开始沉淀时的pH | 沉淀完全的pH |
| Al3+ | 3.4 | 4.7 |
| Cu2+ | 4.1 | 6.9 |
| Mg2+ | 9.4 | 12.4 |
设计如下方案并进行实验:

①调节pH时,应控制pH的范围是pH≥12.4.
②选用NaOH溶液调节pH,得到溶液B的离子方程式是Al3++4OH-=AlO2-+2H2O.
③Al(OH)3经过滤、洗涤、灼烧至恒重后称量,质量为8.5g,则该合金中铝的质量分数是90%.
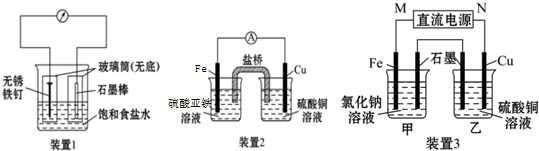
 下列各种物质,有的具有多个官能团:请填写下列空白(填编号):
下列各种物质,有的具有多个官能团:请填写下列空白(填编号):