题目内容
1.在常温常压下,10mL硫化氢气体和一定体积的氧气混合点燃,反应后恢复至原状态,余下15mL气体,则反应前氧气的体积为多少mL?分析 可能发生2H2S+O2$\frac{\underline{\;点燃\;}}{\;}$2S+2H2O或2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O,常温下水为液体,则余下15mL气体为氧气或二氧化硫和氧气的混合气体,以此计算.
解答 解:若发生2H2S+O2$\frac{\underline{\;点燃\;}}{\;}$2S+2H2O,剩余气体为氧气,参加反应的氧气为10mL×$\frac{1}{2}$=5mL,反应前氧气的体积为15ml+5mL=20mL;
若发生2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O,二氧化硫和氧气的混合气体,参加反应的氧气为10mL×$\frac{3}{2}$=15mL,生成二氧化硫为10mL,反应前氧气的体积为15ml+5mL=20mL,
答:反应前氧气的体积为20mL.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应及剩余气体的成分为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
11.下列实验操作或所记录的数据合理的是( )
| A. | NaOH溶液可保存在玻璃塞的试剂瓶中 | |
| B. | 液溴应盛放在用水密封且用玻璃塞塞紧的棕色试剂瓶中 | |
| C. | 配制500ml 0.1mol/L的NaOH溶液时,应用托盘天平称取2.00g NaOH固体 | |
| D. | 氢氟酸可保存在棕色玻璃瓶中 |
12.下列各组离子,在水溶液中能大量共存的是( )
| A. | Na+、Ag+、Cl- | B. | Ba2+、H+、CO32- | C. | K+、Al3+、OH- | D. | Na+、Cl-、NO3- |
9.CoCl2•6H2O是一种饲料营养强化剂.以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种新工艺流程如图:
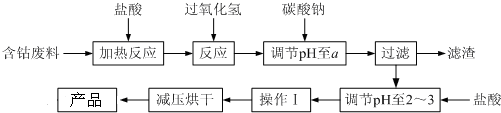
已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
请回答下列问题:
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为减少氮氧化合物等有毒气体的排放,防止产品中混有硝酸盐.
(2)加入过氧化氢的作用是将Fe2+氧化成Fe3+.
(3)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(4)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(5)为测定产品中CoCl2•6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2•6H2O的质量分数大于100%,其原因可能是样品中含有NaCl杂质(或烘干时失去了部分结晶水).

已知:①钴与盐酸反应的化学方程式为:Co+2HCl=CoCl2+H2↑
②CoCl2•6H2O熔点86℃,易溶于水、乙醚等;常温下稳定无毒,加热至110~120℃时,失去结晶水变成有毒的无水氯化钴.
③部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 7.6 | 3.4 |
| 完全沉淀 | 4.1 | 9.7 | 9.2 | 5.2 |
(1)在上述新工艺中,用“盐酸”代替原工艺中“盐酸与硝酸的混酸”直接溶解含钴废料,其主要优点为减少氮氧化合物等有毒气体的排放,防止产品中混有硝酸盐.
(2)加入过氧化氢的作用是将Fe2+氧化成Fe3+.
(3)加入碳酸钠调节pH至a,a的范围是5.2~7.6.
(4)操作Ⅰ包含3个基本实验操作,它们是蒸发浓缩、冷却结晶和过滤.
(5)为测定产品中CoCl2•6H2O含量,某同学将一定量的样品溶于水,再向其中加入足量的AgNO3溶液,过滤,并将沉淀烘干后称量其质量.通过计算发现产品中CoCl2•6H2O的质量分数大于100%,其原因可能是样品中含有NaCl杂质(或烘干时失去了部分结晶水).
16.下列微粒的基态电子排布式一定错误的是( )
| A. | A原子:1s22s22p63s23p63d10 | B. | B2-:1s22s22p6 | ||
| C. | C2+:1s22s22p6 | D. | D原子:1s22s22p6 |
8.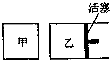 在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,
在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,
若甲容器的容积不变,乙容器的压强不变,甲中S02的转化率为a%,乙容器中SO2的转化率为b%,则a与b的关系为( )
 在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,
在容积相同的甲、乙两个容器中(如图所示),分别充入2molSO2和2molO2,使它们在相同温度下发生反应2SO2(g)+O2(g)?2SO3(g)并达到平衡.在反应过程中,若甲容器的容积不变,乙容器的压强不变,甲中S02的转化率为a%,乙容器中SO2的转化率为b%,则a与b的关系为( )
| A. | a>b | B. | a=b | C. | a<b | D. | 无法确定 |
5.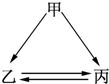 下列各组物质不能一步实现如图转化关系的是( )
下列各组物质不能一步实现如图转化关系的是( )
 下列各组物质不能一步实现如图转化关系的是( )
下列各组物质不能一步实现如图转化关系的是( )| 物质 组别 | 甲 | 乙 | 丙 |
| A | Na | NaOH | NaCl |
| B | AlO3 | Na AlO2 | Al(OH)3 |
| C | CuO | Cu(OH)2 | CuSO4 |
| D | Fe | FeCl3 | FeCl2 |
| A. | A | B. | B | C. | C | D. | D |
6.下列图示与对应的叙述相符的是( )
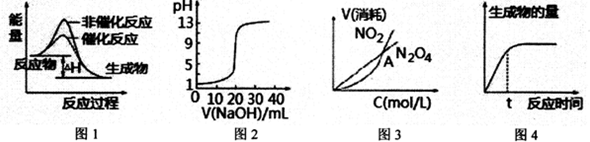

| A. | 图l表示某吸热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| B. | 图2表示0.1000mol•L-1NaOH溶液滴定20.00mL0.1 000mol•L-1 CH3COOH溶液所得到的滴定曲线 | |
| C. | 图3表示恒温恒容条件下,2NO2(g)?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| D. | 图4表示某可逆反应生成物的量随反应时间变化的曲线,由图知t时v正>v逆 |