��Ŀ����
15��ij��Ӳ���Ͻ����� Al��Cu��Mg���ֽ�����ɣ���ҪӦ�������ȿɺ��Ľṹ�����ͼ���ij�о�С����̽���úϽ�����ʲ��ⶨ�Ͻ�������������������1����ͬѧԤ�⣺�úϽ���10mol/L���ᷴӦʱ��NO2�������ɣ����ܻ���NO���ɣ�
�������ϣ������£�NO2��N2O4��ϴ��ڣ��ڵ���0��ʱ����ֻ����ɫ��N2O4Һ�������ڣ��������װ�ý���ʵ�飮��ͼ����װ�ò����������Ժ�ȡ5g �Ͻ����Բ����ƿ�У����μ�10mol/L���ᣮ
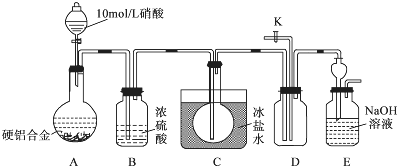
�ٺϽ���Cu��ϡ���ᷴӦ�����ӷ���ʽ��3Cu+2NO3-+8H+=Cu2++2NO��+4H2O��
��Cװ�õ�Ŀ���ǽ����ɵ�NO2����ΪN2O4����NO���룬�ų����ţ�
����֤����NO���ɵ�ʵ������������Ǵ���K�������������D�е���������ɫ��Ϊ����ɫ��֤����NO���ɣ�
��ʵ�������A�й���ȫ���ܽ��δ���鵽��NO���ɣ���ͬѧ��ΪӲ���Ͻ���10mol/L���ᷴӦʱû��NO���ɣ���ͬѧ��Ϊ����ȷ���Ƿ�������NO���貹���������֤�����ò������ڼ���HNO3ǰ��ͨ��N2������װ���еĿ�����
��2��Ϊ�ⶨ�Ͻ�������������������ͬѧ�������ϣ�
���ֽ������������������������pH
| �������� | ��ʼ����ʱ��pH | ������ȫ��pH |
| Al3+ | 3.4 | 4.7 |
| Cu2+ | 4.1 | 6.9 |
| Mg2+ | 9.4 | 12.4 |
������·���������ʵ�飺

�ٵ���pHʱ��Ӧ����pH�ķ�Χ��pH��12.4��
��ѡ��NaOH��Һ����pH���õ���ҺB�����ӷ���ʽ��Al3++4OH-=AlO2-+2H2O��
��Al��OH��3�����ˡ�ϴ�ӡ����������غ����������Ϊ8.5g����úϽ�����������������90%��
���� ��1����ͭ��ϡ���ᷴӦ��������ͭ��һ�����������ˮ��
�ڸ��ݡ������£�NO2��N2O4��ϴ��ڣ��ڵ���0��ʱ����ֻ����ɫ��N2O4Һ�������ڡ���ʵ��Ŀ�ķ�����
�۶�������Ϊ����ɫ���壬���Ը���A������������ɫ��C���Ƿ��й��������жϣ�D��ͨ����������ɫ�����Ϊ����ɫ����֤�����ɵ������к���NO��
��NO�ܹ��������������Ӧ���ɶ���������Ӱ���ʵ��ⶨ��
��2���ٸ��ݷ�Ӧ���̿�֪����ҺB�к���ƫ��������ӣ�����CΪ������þ��������ͭ�����Ե��ڵ���Һ��pH����ʹ����������ȫ�ܽ⣻
����ҺB�к���ƫ��������ӣ�������ӦΪ�����������������ӷ�Ӧ����ƫ��������Ӻ�ˮ��
����������������������������������������������������ӵ����ʵ������ټ�����Ͻ�����������������
��� �⣺��1����ͭ��ϡ���ᷴӦ����NO���壬��Ӧ�����ӷ���ʽΪ��3Cu+2NO3-+8H+=3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+2NO3-+8H+=3Cu2++2NO��+4H2O��
����֪�����£�NO2��N2O4��ϴ��ڣ��ڵ���0��ʱ����ֻ����ɫ��N2O4Һ�������ڣ���ʵ��Ŀ���Ǽ������ɵ������к���NO������װ��C�������ǽ����ɵ�NO2����ΪN2O4����NO���룬�ų����ţ�
�ʴ�Ϊ�������ɵ�NO2����ΪN2O4����NO���룬�ų����ţ�
����A���к���ɫ���������ɣ�C������ɫ��Һ�������ڣ���֤����Ӧ���ж��������������ɣ���֤����NO���ɵ�ʵ�����������Ϊ������K�������������D�е���������ɫ��Ϊ����ɫ��֤����NO���ɣ�
�ʴ�Ϊ������K�������������D�е���������ɫ��Ϊ����ɫ��֤����NO���ɣ�
������װ����������NO��Ӧ���ɶ���������������ʵ�飬����Ӧ�ü���HNO3ǰ��ͨ��N2������װ���еĿ�����
�ʴ�Ϊ���ڼ���HNO3ǰ��ͨ��N2������װ���еĿ�����
��2���ٽ�Ϸ�Ӧ���̿�֪����ҺB�к���ƫ��������ӣ�����CΪ������þ��������ͭ���������Һ��pH�������㣬þ���ӡ�ͭ������ȫ����������������ȫת����ƫ��������ӣ����ݱ������ݼ�����������ȫ�ܽ��pH��֪����ʱ��pHpH��12.4��
�ʴ�Ϊ��pH��12.4��
����ҺB�к���ƫ��������ӣ���Ӧ�����ӷ���ʽΪ��Al3++4OH-=AlO2-+2H2O��
�ʴ�Ϊ��Al3++4OH-=AlO2-+2H2O��
��8.5gΪ���������������������������ʵ���Ϊ��$\frac{8.5g}{102g/mol}$��0.0833mol�����������غ��֪�Ͻ��к����������ʵ���Ϊ��0.0833mol��2=0.1666mol�����ԺϽ���������������Ϊ��$\frac{27g/mo��0.1666mol}{5g}$��100%��90.0%��
�ʴ�Ϊ��90.0%��
���� ���⿼����̽��������ɡ��������ʺ����ķ�������Ŀ�ѶȽϴ�����֪ʶ��϶ࡢ�ۺ��Խ�ǿ����ֿ�����ѧ���ķ�����������������ѧ������������ȷ�ⶨԭ��Ϊ���ؼ���ע���������ջ�ѧʵ���������������

 Сѧ�̲�ȫ��ϵ�д�
Сѧ�̲�ȫ��ϵ�д� Сѧ��ѧ������ѿڶ���ϵ�д�
Сѧ��ѧ������ѿڶ���ϵ�д� ������Ӧ�������������ϵ�д�
������Ӧ�������������ϵ�д� �㽭֮�ǿ�ʱ�Ż���ҵϵ�д�
�㽭֮�ǿ�ʱ�Ż���ҵϵ�д�| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �٢ڢ� | D�� | �٢ڢۢ� |
| A�� | �γ����� | B�� | ʹȫ�������ů | C�� | �ƻ������� | D�� | ������ |
| A�� | ��״���£�11.2 L CCl4�����ķ�����Ϊ0.5 NA | |
| B�� | ���³�ѹ�£�4.2 g C2H4��C8H16�Ļ�����к��е�̼ԭ����Ϊ0.3 NA | |
| C�� | 7.8 g��������̼̼˫������ĿΪ0.3 NA | |
| D�� | 6.4 g Cu��20 mL 10 mol•L-1Ũ���ᷴӦ��ת�Ƶĵ�����Ϊ0.2 NA |
| A�� | ����һ�ַ�ɢϵ����ɢ���ǹ��� | |
| B�� | ����һ�ַ�ɢϵ����ɢ�������� | |
| C�� | �����ڽ����ɢϵ | |
| D�� | �������������в������ﳾ���Լ��������������γ� |
| A�� | �κ�����Ӧ����1 mol H2O�Ĺ����У��ų�����������ͬ | |
| B�� | �������������������ֱ���ȫȼ�գ�ǰ�߷ų������� | |
| C�� | ����ʱ��H2��g��+Cl2��g���T2HCl��g����H=aKJ/mol������Ӧ������Ϊ��ȼ����H������ | |
| D�� | ��ʾ̼ȼ���ȵ��Ȼ�ѧ����ʽΪ��2C��s��+O2��g���T2CO��g����H=-221kJ•mol-1 |
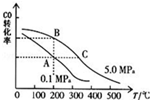 �״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ش���������
�״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ش���������