2.在室温下,等体积的酸和碱溶液混合后pH一定小于7的是( )
| A. | pH=3的HNO 3与pH=11的KOH溶液 | |
| B. | pH=3的HNO 3与pH=11的氨水 | |
| C. | pH=3的H 2SO 4与pH=11的NaOH溶液 | |
| D. | pH=3的CH 3COOH与pH=11的Ba(OH) 2溶液 |
1.下列事实能说明亚硝酸是弱电解质的是( )
| A. | pH=4的亚硝酸溶液c(H+)=1×10-4mol/L | |
| B. | 用亚硝酸溶液作导电实验,灯泡很暗 | |
| C. | 将Vml pH=4的亚硝酸稀释成pH=5的溶液,所需加入的水量大于10Vml | |
| D. | 10mL 1mol/L的亚硝酸恰好与10mL 1mol/L NaOH溶液完全中和 |
20.下列有关化学反应速率的说法中,正确的是( )
| A. | 100 mL 1 mol/L 的稀硫酸与锌反应时,加入适量的氯化钠溶液,生成氢气的速率不变 | |
| B. | 合成氨的反应是一个放热反应,所以升高温度,反应速率减慢 | |
| C. | 用铁片和稀硫酸反应制取氢气时,改用铁片和浓硫酸可以加快产生氢气的速率 | |
| D. | 汽车尾气中的 CO 和 NO 可以缓慢反应生成 N2和 CO2,减小压强,反应速率减慢 |
19.下列事实中,能用勒沙特列原理来解释的是( )
| A. | 由H 2(g)、I 2(g)、HI(g)组成的混合气体平衡体系加压后颜色加深 | |
| B. | 久置的氯水变成了稀盐酸 | |
| C. | 在FeCl 3溶液中加入铁粉防止氧化变质 | |
| D. | 加入催化剂有利于SO 2与O 2反应制SO 3 |
18.标准状态下,气态分子断开1mol化学键的焓变称为键焓.已知H-H、H-O和O═O键的键焓△H分别为436kJ•mol - 1、463kJ•mol - 1和495kJ•mol - 1.下列热化学方程式正确的是( )
| A. | H 2O(g)═H 2(g)+O 2(g)△H=-485 kJ•mol - 1 | |
| B. | H 2O(g)═H 2(g)+O 2(g)△H=+485 kJ•mol - 1 | |
| C. | 2H 2(g)+O 2(g)═2H 2O(g)△H=+485 kJ•mol - 1 | |
| D. | 2H 2(g)+O 2(g)═2H 2O(g)△H=-485 kJ•mol - 1 |
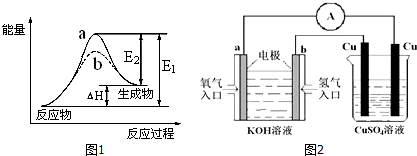
17.某反应过程能量变化如图所示,下列说法正确的是( )


| A. | 改变催化剂,可改变该反应的活化能 | |
| B. | 该反应为放热反应,热效应等于E 1-E 2 | |
| C. | 反应过程 a 有催化剂参与 | |
| D. | 有催化剂条件下,反应的活化能等于 E 1+E 2 |
16.下列设备工作时,将化学能转化为热能的是( )
0 153476 153484 153490 153494 153500 153502 153506 153512 153514 153520 153526 153530 153532 153536 153542 153544 153550 153554 153556 153560 153562 153566 153568 153570 153571 153572 153574 153575 153576 153578 153580 153584 153586 153590 153592 153596 153602 153604 153610 153614 153616 153620 153626 153632 153634 153640 153644 153646 153652 153656 153662 153670 203614
| A. |  太阳能生热器 | B. |  硅太阳能电池 | C. |  燃气灶 | D. |  锂离子电池 |