2.浙江大学成功研制出能在数分钟之内将电量充满的锂电池,其成本只有传统锂电池的一半.若电解液为LiAlCl4-SOCl2,电池的总反应为:4Li+2SOCl2$\frac{\underline{\;充电\;}}{放电}$4LiCl+S+SO2.下列说法正确的是( )
| A. | 充电时阳极反应式为:4Cl-+S+SO2-4e-═2SOCl2 | |
| B. | 电池的电解液可用LiCl水溶液代替 | |
| C. | 放电时电子从负极经电解液流向正极 | |
| D. | 该电池放电时,负极发生还原反应 |
1.下列有关说法不正确的是( )
| A. | 25℃时,0.1mol•L-1的三种溶液的pH关系为:pH(Na2CO3)>pH(NaHCO3)>pH(CH3COONa) | |
| B. | 25℃时,pH=5的CH3COOH溶液和pH=5的NH4Cl溶液,c(H+)相等 | |
| C. | 25℃时,BaCO3在纯水中的KSP比在Na2CO3溶液中的KSP大 | |
| D. | NaHCO3和Na2CO3混合溶液中,一定有c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
19.已知H2(g)+I2(g)?2HI(g)△H<0,有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各1mol,乙中加入HI2mol,相同温度下分别达到平衡,欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
| A. | 甲、乙提高相同温度 | B. | 甲中加入1molHe,乙不变 | ||
| C. | 甲降低温度,乙不变 | D. | 甲增加1molH2,乙增加1molI2 |
18.下列有关惰性电极电解AgNO3溶液一段时间后的说法,正确的是( )
| A. | 电解过程中阴极质量不变 | |
| B. | 电解过程中溶液的pH不断升高 | |
| C. | 此时向溶液中加入适量的Ag2O固体可使溶液恢复电解前的状况 | |
| D. | 电解后两极产生的气体体积比为2:1 |
17.下列实验误差分析正确的是( )
| A. | 用湿润的pH试纸测稀碱液的pH,测定值偏大 | |
| B. | 用容量瓶配制溶液,定容时俯视刻度线,所配溶液浓度偏小 | |
| C. | 滴定前滴定管内无气泡,终点读数时有气泡,所测体积偏小 | |
| D. | 测定中和反应反的应热时,将碱缓慢倒入酸中,所测温度值偏大 |
16.某溶液中可能含有I-、NH4+、Cu2+、SO32-,向溶液中加入足量的溴水,反应后溶液仍呈无色,则下列关于溶液组成的判断正确的是( )
0 153431 153439 153445 153449 153455 153457 153461 153467 153469 153475 153481 153485 153487 153491 153497 153499 153505 153509 153511 153515 153517 153521 153523 153525 153526 153527 153529 153530 153531 153533 153535 153539 153541 153545 153547 153551 153557 153559 153565 153569 153571 153575 153581 153587 153589 153595 153599 153601 153607 153611 153617 153625 203614
| A. | 肯定不含I- | B. | 肯定不含NH4+ | C. | 肯定不含Cu2+ | D. | 肯定不含SO32- |
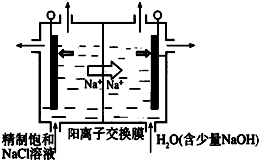 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺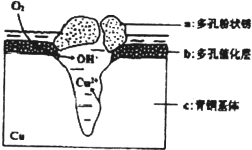 我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义.
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器因受到环境腐蚀,欲对其进行修复和防护具有重要意义. 甲醇是人们开发和利用的一种新能源.已知:
甲醇是人们开发和利用的一种新能源.已知: