题目内容
19.已知H2(g)+I2(g)?2HI(g)△H<0,有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各1mol,乙中加入HI2mol,相同温度下分别达到平衡,欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )| A. | 甲、乙提高相同温度 | B. | 甲中加入1molHe,乙不变 | ||
| C. | 甲降低温度,乙不变 | D. | 甲增加1molH2,乙增加1molI2 |
分析 同容积的定容密封容器甲和乙,甲中加入H2和I2各1mol,乙中加入HI 2mol,由于乙按化学计量数转化到左边,可以得到H2和I2各1mol,故此时甲和乙建立的平衡是等效的,欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取措施使平衡向正反应移动,但不能降低HI的浓度,然后结合影响化学平衡移动的因素来回答.
解答 解:相同容积的定容密封容器甲和乙,甲中加入H2和I2各1mol,乙中加入HI2mol,此时甲和乙建立的平衡是等效的,
A.甲、乙提高相同温度,平衡均逆向移动,HI的平衡浓度均减小,故A错误;
B.甲中加人1molHe,在定容密封容器中,平衡不会移动,故B错误;
C.甲降低温度,平衡正向移动,甲中HI的平衡浓度增大,乙不变,可以满足甲中HI的平衡浓度大于乙中HI的平衡浓度,故C正确;
D.甲中增加1molH2,乙增加1molI2,结果还是等效的,达到平衡时HI的浓度相等,故D错误;
故选C.
点评 本题考查化学平衡及其影响,侧重考查等效平衡知识,题目难度中等,明确化学平衡及其影响因素为解答关键,试题培养了学生的分析能力及灵活应用能力.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
7.乙醇是一种重要的化工原料,在人们日常生活中有广泛应用.下列关于乙醇的说法不正确的是( )
| A. | 无色液体 | B. | 可以被氧化 | ||
| C. | 能与水以任意比例混溶 | D. | 能与氢氧化钠溶液反应 |
14.下列有关元素化合物的说法正确的是( )
| A. | 常温下,1mol铜片投入含有4mol HNO3的浓硝酸中,铜片可以完全溶解 | |
| B. | Al与S直接化合可以得到Al2S3,Fe与S直接化合也可以得到Fe2S3 | |
| C. | 电解AlCl3、FeCl3、CuCl2的混合溶液中,阴极上依次析出Cu、Fe、Al | |
| D. | 等质量的钠铝合金中铝的含量越大,与足量盐酸反应时放出的氢气越少 |
11.过渡元素在生活、生产和科技等方面有广泛的用途.
(1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般而言,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色,据此判断,[Mn(H2O)6]2+有(填“有”或“无”)颜色.
(2)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子.下列说法中不正确的是D.(填序号)
A.PFS中铁显+3价
B.铁原子的外围电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用.现有铬(Ⅲ)与甲基丙烯酸根的配合物为:{Cr2[OOC-C(CH3)═CH2]2(H2O)8}Cl4
①该化合物中存在的化学键类型有配位键、共价键、离子键.
②甲基丙烯酸分子中C原子的杂化方式有sp3和sp2.
③等电子体是具有相同的价电子数和原子数的分子或离子,与H2O分子互为等电子体的微粒是H2S(填一种即可).
④与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是K、Cu(填元素符号).
(1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关.一般而言,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色,据此判断,[Mn(H2O)6]2+有(填“有”或“无”)颜色.
(2)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子.下列说法中不正确的是D.(填序号)
A.PFS中铁显+3价
B.铁原子的外围电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
| 元素 | Mn | Fe | |
| 电离能 | I1 | 717 | 759 |
| (kJ•mol-1) | I2 | 1 509 | 1 561 |
| I3 | 3 248 | 2 957 | |
①该化合物中存在的化学键类型有配位键、共价键、离子键.
②甲基丙烯酸分子中C原子的杂化方式有sp3和sp2.
③等电子体是具有相同的价电子数和原子数的分子或离子,与H2O分子互为等电子体的微粒是H2S(填一种即可).
④与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是K、Cu(填元素符号).
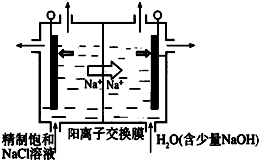 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.目前已开发出用电解法制取ClO2的新工艺
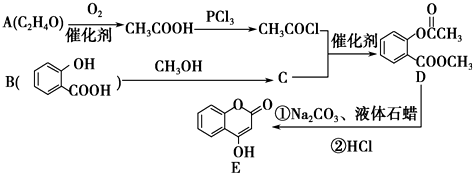
 +2NaOH $\stackrel{△}{→}$
+2NaOH $\stackrel{△}{→}$  +H2O.
+H2O. 是一种重要的有机合成中间体.
是一种重要的有机合成中间体. ;②光照时,甲苯与Cl2侧链取代.
;②光照时,甲苯与Cl2侧链取代.