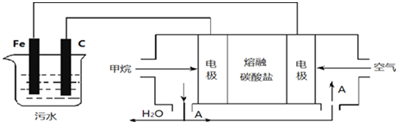
11.下列关于电解池的说法正确的是( )
| A. | 电源的负极就是阴极 | |
| B. | 与直流电源正极相连的是电解池的阴极 | |
| C. | 与直流电源负极相连的电极上发生还原反应 | |
| D. | 阳极上发生还原反应 |
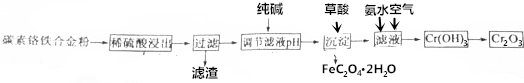
9.某同学为了验证Fe3+是否能氧化H2SO3生成了SO42-,他用50mL0.1mol/LFeCl3溶液吸收制取SO2气体的尾气,再进行以下实验:
(1)向FeCl3溶液中通入一定量的SO2,反应的离子方程式:SO2+2H20+2Fe3+=2Fe2++SO42-+4H+
(2)检验吸收液中SO42-的方法:取少量样品溶液于试管中,先滴入足量的稀盐酸,再滴入氯化钡溶液,有白色沉淀生成
(3)吸收液中除了含有H+、Cl-、SO42-以外,对其它成份(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设.
假设1:溶液中存在Fe3+、Fe2+;
假设2:溶液中存在Fe2+、H2SO3
假设3:溶液中存在Fe2+而不存在H2SO3 (二者恰好完全反应).
②设计方案、进行实验,验证假设.请在表中写出实验步骤以及预期现象和结论(可以不填满).限选实验试剂和仪器:试管、滴管、0.1moL•L-1KMnO4、0,.1moL•L-1KSCN溶液、品红溶液.
0 153398 153406 153412 153416 153422 153424 153428 153434 153436 153442 153448 153452 153454 153458 153464 153466 153472 153476 153478 153482 153484 153488 153490 153492 153493 153494 153496 153497 153498 153500 153502 153506 153508 153512 153514 153518 153524 153526 153532 153536 153538 153542 153548 153554 153556 153562 153566 153568 153574 153578 153584 153592 203614
(1)向FeCl3溶液中通入一定量的SO2,反应的离子方程式:SO2+2H20+2Fe3+=2Fe2++SO42-+4H+
(2)检验吸收液中SO42-的方法:取少量样品溶液于试管中,先滴入足量的稀盐酸,再滴入氯化钡溶液,有白色沉淀生成
(3)吸收液中除了含有H+、Cl-、SO42-以外,对其它成份(Fe3+、Fe2+、H2SO3)的可能组合进行探究:
①提出假设.
假设1:溶液中存在Fe3+、Fe2+;
假设2:溶液中存在Fe2+、H2SO3
假设3:溶液中存在Fe2+而不存在H2SO3 (二者恰好完全反应).
②设计方案、进行实验,验证假设.请在表中写出实验步骤以及预期现象和结论(可以不填满).限选实验试剂和仪器:试管、滴管、0.1moL•L-1KMnO4、0,.1moL•L-1KSCN溶液、品红溶液.
| 实验步骤 | 预期现象和结论 |
| 步骤1:用试管取样品溶液2~3mL,再用滴管取LKSCN溶液,向试管中滴入1~2滴0.1mol/LKSCN溶液 | (1)若出现红色,则假设1成立; (2)若未出现红色,则假设2或假设3成立. |
步骤2:另取2~3mL样品溶液于试管中滴入1~2mL品红稀溶液 | 1若品红溶液红色褪色,假设2成立; 2若品红溶液不褪色,结合步骤1中的(2)则假设3成立 |
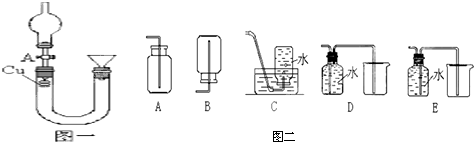

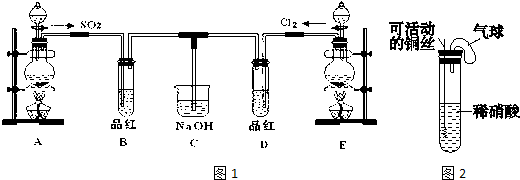
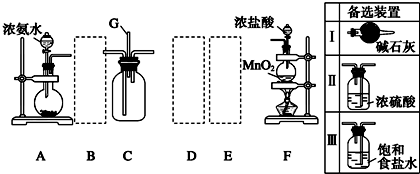
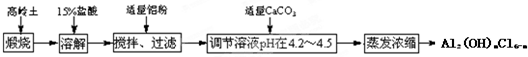
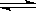 Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a L,试回答:
Z(g)+2W(g)△H<0达到平衡(Ⅰ)时V(B)=0.9a L,试回答: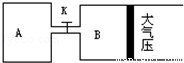
 器恢复原来反应前的体积,可采取的措施是____________________。
器恢复原来反应前的体积,可采取的措施是____________________。