3.铜锌原电池(如图)工作时,下列叙述正确的是( )


| A. | 一段时间后铜片增重,盐桥中K+移向CuSO4溶液 | |
| B. | 正极反应为:Zn-2e-═Zn2+ | |
| C. | 电子从铜片经导线流向锌片 | |
| D. | 电池工作时Zn2+和Cu2+ 的浓度保持不变 |
2.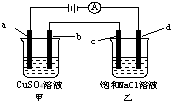 如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
 如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )
如图所示,a、b、c均为石墨电极,d为碳钢电极,通电电解一段时间.假设在电解过程中产生的气体全部逸出,下列说法正确的是( )| A. | 甲、乙两烧杯中溶液的pH均保持不变 | |
| B. | 当b极增重3.2 g时,d极产生的气体为0.56 L(标准状况) | |
| C. | 当电解一段时间后,将甲、乙两溶液混合,一定会产生蓝色沉淀 | |
| D. | 甲烧杯中a电极反应式为:4OH--4e-═O2↑+2H2O |
1.下列反应中,不能形成原电池反应的是( )
| A. | 氢氧化钠与盐酸反应 | B. | 金属锌与稀硫酸反应 | ||
| C. | 甲烷燃烧 | D. | 金属铜溶于氯化铁溶液 |
20.铅蓄电池是典型的可充电电池,在现代生活中有着广泛的应用,其充电、放电按下式进行:Pb+PbO2+2H2SO4$?_{充电}^{放电}$2PbSO4+2H2O,有关该电池的说法正确的( )
| A. | 放电时,电解质溶液的pH不断降低且正负极均有PbSO4 生成 | |
| B. | 放电时,每通过1mol电子,蓄电池就要消耗2mol H2SO4 | |
| C. | 充电时,阳极反应:PbSO4+2e-=Pb+SO42- | |
| D. | 充电时,铅蓄电池的负极与外接电源的负极相连 |
19.以Mg片和Al片为电极,并用导线连接,同时插入NaOH溶液中,下列说法正确的是( )
| A. | Mg片作负极,电极反应:Mg-2e-═Mg2+ | |
| B. | Al片作负极,电极反应:Al+4OH--3e-═AlO2-+2H2O | |
| C. | 电子从Mg电极沿导线流向Al电极 | |
| D. | Al片上有气泡产生 |
18.下列说法不正确的是( )
| A. | 原电池外电路中电子由负极流向正极 | |
| B. | 原电池中发生还原反应的电极是正极 | |
| C. | 电解池中发生还原反应的电极是阳极 | |
| D. | 电解池中质量增加的电极是阴极 |
17.某同学用图所示的装置及药品进行比较酸性强弱的实验,下列说法不正确的是( )
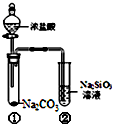

| A. | 向Na2SiO3溶液中直接滴入盐酸溶液无明显现象 | |
| B. | 试管①中反应的离子方程式是:Na2CO3+2H+═2Na++CO2↑+H2O | |
| C. | 该实验可以证明酸性:盐酸>碳酸>硅酸 | |
| D. | 一段时间后试管②中有胶冻状物质生成 |
16.从下列事实所列出的相应结论合理的是( )
| A. | SO2的水溶液可以导电说明是SO2电解质 | |
| B. | 加热NaOH溶液时不能使用玻璃试管,因为玻璃中的SiO2能与NaOH反应 | |
| C. | 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,该溶液一定有NH4+ | |
| D. | 某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中一定含有CO32-或HCO3- |
15.5种固体物质A、B、C、D、E由下表中不同的阴阳离子组成,它们均易溶于水.
分别取它们的水溶液进行实验,结果如下:
①C,E溶液显碱性,A,B,D溶液呈酸性,0.1mol/L的E溶液PH<13;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④将38.4g Cu片投入装有足量D溶液的试管中,Cu不溶解,再滴加1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断C、D的化学式为:CBa(OH)2;DAl(NO3)3.
(2)写出步骤②中发生反应的离子反应方程式2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(3)步骤④中若要将Cu片完全溶解,至少加入稀H2SO4的体积是500mL.
(4)不能确定的溶液为B和A(填字母编号).
| 阳离子 | Na+、Al 3+、Fe3+、Cu2+、Ba2+ |
阴离子 | OH-、Cl-、CO32-、NO3-、SO4- |
①C,E溶液显碱性,A,B,D溶液呈酸性,0.1mol/L的E溶液PH<13;
②B溶液与E溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量C溶液与D溶液混合后产生白色沉淀,过量C溶液与D溶液混合后无现象;
④将38.4g Cu片投入装有足量D溶液的试管中,Cu不溶解,再滴加1.6mol•L-1稀H2SO4,Cu逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断C、D的化学式为:CBa(OH)2;DAl(NO3)3.
(2)写出步骤②中发生反应的离子反应方程式2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑.
(3)步骤④中若要将Cu片完全溶解,至少加入稀H2SO4的体积是500mL.
(4)不能确定的溶液为B和A(填字母编号).
14.可逆反应FeCl3+3KSCN?Fe(SCN)3+3KCl达到化学平衡后,加人少量的水,平衡的移动情况为( )
0 153273 153281 153287 153291 153297 153299 153303 153309 153311 153317 153323 153327 153329 153333 153339 153341 153347 153351 153353 153357 153359 153363 153365 153367 153368 153369 153371 153372 153373 153375 153377 153381 153383 153387 153389 153393 153399 153401 153407 153411 153413 153417 153423 153429 153431 153437 153441 153443 153449 153453 153459 153467 203614
| A. | 不移动 | B. | 平衡左移 | C. | 平衡右移 | D. | 无法确定 |