16.在密闭容器中进行的反应:N2+3H2?2NH3,下列说法正确的是( )
| A. | 加入催化剂能加快反应速率 | |
| B. | 增大压强能减慢反应速率 | |
| C. | 达到平衡时,反应速率:v(正)=v(逆)=0 | |
| D. | 达到平衡时,N2和H2能100%转化为NH3 |
15.某溶液中可能含有Cl-、SO42-、CO32-、NH4+、Fe3+和Na+.某同学为确定其组分,设计并完成了如下实验:
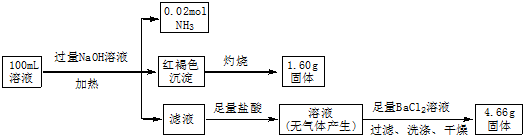
由此可推测原溶液中( )

由此可推测原溶液中( )
| A. | SO42-、NH4+和Na+ 一定存在,CO32-一定不存在 | |
| B. | SO42-、NH4+一定存在,Na+ 和CO32-一定不存在 | |
| C. | c(Fe3+)=0.1 mol•L-1 | |
| D. | c(Cl-)≥0.4mol•L-1 |
14.下列关于物质或离子检验的叙述正确的是( )
| A. | 向某溶液中加入BaCl2溶液,出现白色沉淀,再加稀硝酸溶液,若沉淀不溶解,则该溶液中肯定有SO42- | |
| B. | 灼烧某白色粉末,火焰呈黄色,则证明原粉末中肯定有Na+,无K+ | |
| C. | 向某溶液中滴加AgNO3溶液后,出现白色沉淀,再加稀盐酸,若沉淀不溶解,则证明溶液中肯定有Cl- | |
| D. | 在某盐溶液中加入氢氧化钠浓溶液,加热,产生的气体能使湿润的红色石蕊试纸变蓝,则该溶液中肯定有NH4+ |
13.I 铜是人类最早使用的金属,它与人类生产生活关系密切,请运用所学知识解释下列与铜有关的化学现象.

(1)如图甲,在硫酸型酸雨地区,不纯的铜制品发生电化学腐蚀,Cu发生氧化反应(填写“氧化”或“还原”),写出正极的电极反应式O2+4H++4e-=2H2O;
(2)如图乙,将螺旋状的铜丝在酒精灯上灼烧,铜丝变黑色,然后将红热的铜丝插入NH4Cl固体中,过一会取出,发现插入部分的黑色变为光亮的红色,查阅资料可知,该过程有N2生成,写出由黑色变为光亮红色过程的反应方程式2NH4Cl+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2↑+2HCl+3H2O;
II 在一个密闭容器中发生反应:mA(g)+nB(g)?pC(g)
(1)该反应未加催化剂的v-t图象如图丙,若其他条件不变,仅在反应前加入合适的催化剂,则其v-t图象如图丁所示.以下说法正确的是②③⑤ (填序号)
①a1>a2
②b1<b2
③t1>t2
④右图中阴影部分面积更大
⑤两图中阴影部分面积相等
(2)在一定温度和不同压强下达到平衡时,分别得到物质A的物质的量浓度如下表
①当压强为2×105 Pa时,此反应的平衡常数表达式:$\frac{{c}^{p}(C)}{{c}^{m}(A){c}^{n}(B)}$.
②当压强从2×105加压到5×105时,平衡的移动方向是C.
A.朝正反应方向移动 B.朝逆反应方向移动 C.不移动 D.不能确定
③其他条件相同时,在上述三个压强下分别发生该反应.2×105 Pa时,A的转化率随时间变化如图2,请在图中补充画出压强分别为5×105 Pa 和1×106 Pa时,A的转化率随时间的变化曲线(请在图线上标出压强).

(1)如图甲,在硫酸型酸雨地区,不纯的铜制品发生电化学腐蚀,Cu发生氧化反应(填写“氧化”或“还原”),写出正极的电极反应式O2+4H++4e-=2H2O;
(2)如图乙,将螺旋状的铜丝在酒精灯上灼烧,铜丝变黑色,然后将红热的铜丝插入NH4Cl固体中,过一会取出,发现插入部分的黑色变为光亮的红色,查阅资料可知,该过程有N2生成,写出由黑色变为光亮红色过程的反应方程式2NH4Cl+3CuO$\frac{\underline{\;\;△\;\;}}{\;}$3Cu+N2↑+2HCl+3H2O;
II 在一个密闭容器中发生反应:mA(g)+nB(g)?pC(g)
(1)该反应未加催化剂的v-t图象如图丙,若其他条件不变,仅在反应前加入合适的催化剂,则其v-t图象如图丁所示.以下说法正确的是②③⑤ (填序号)
①a1>a2
②b1<b2
③t1>t2
④右图中阴影部分面积更大
⑤两图中阴影部分面积相等
(2)在一定温度和不同压强下达到平衡时,分别得到物质A的物质的量浓度如下表
| 压强p/Pa | 2×105 | 5×105 | 1×106 |
| c(A)/mol•L-1 | 0.08 | 0.20 | 0.44 |
②当压强从2×105加压到5×105时,平衡的移动方向是C.
A.朝正反应方向移动 B.朝逆反应方向移动 C.不移动 D.不能确定
③其他条件相同时,在上述三个压强下分别发生该反应.2×105 Pa时,A的转化率随时间变化如图2,请在图中补充画出压强分别为5×105 Pa 和1×106 Pa时,A的转化率随时间的变化曲线(请在图线上标出压强).
12.在一定温度下反应:2NO2(g)═N2O4(g)△H<0,其化学平衡常数为K,则下列说法正确的是( )
| A. | 相同温度,2N2O4(g)═4NO2(g)的反应热和化学平衡常数分别为-2△H和K2 | |
| B. | 该反应达到平衡后,缩小容器的容积,平衡右移,混合气体颜色变浅 | |
| C. | 若投入2mol NO2,通过控制外界条件,必能生成1mol N2O4 | |
| D. | 平衡时一定有v正(NO2)=2v逆(N2O4) |
10.下列图示与对应的叙述相符的是( )
0 153217 153225 153231 153235 153241 153243 153247 153253 153255 153261 153267 153271 153273 153277 153283 153285 153291 153295 153297 153301 153303 153307 153309 153311 153312 153313 153315 153316 153317 153319 153321 153325 153327 153331 153333 153337 153343 153345 153351 153355 153357 153361 153367 153373 153375 153381 153385 153387 153393 153397 153403 153411 203614
| A. | 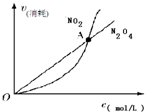 表示在恒容密闭容器中,恒温条件下发生的可逆反应2NO2(g)?N2O4(g),各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| B. | 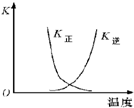 曲线表示反应2A(g)+B(g)?2C(g)△H>0,正、逆反应的平衡常数K随温度的变化 | |
| C. | 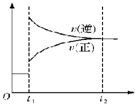 表示对反应2X(g)+Y(g)?Z(s)+3W(g)△H<0 在t1时刻增大压强 | |
| D. | 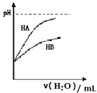 表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH小于NaB溶液pH |
 将漫射日光照射到装有氯气和甲烷混合气体(体积比4:1)的装置上.
将漫射日光照射到装有氯气和甲烷混合气体(体积比4:1)的装置上.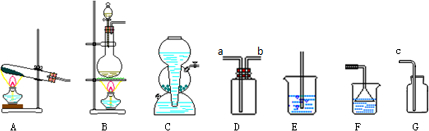
 喷泉实验是一种常见的自然现象,其产生原因是存在压强差.试根据下图,回答下列问题:
喷泉实验是一种常见的自然现象,其产生原因是存在压强差.试根据下图,回答下列问题: