3.NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 100mL、1moL•L-1的ALCL3溶液中,含A13+的数目为0.1 NA | |
| B. | 足量Fe与0.1 mol CL2充分反应,转移的电子数目为0.3 NA | |
| C. | 在02参与的反应中,1mol 02作氧化剂时得到的电子数目一定为4 NA | |
| D. | 2.8g乙烯与一氧化碳的混合气体,所含分子数目为0.1 NA |
2.海水资源丰富,海水中主要含有Na+、K+、Mg2+、Cl-、SO42-、Br-、CO32-、HCO3-等离子.合理利用海水资源和保护环境是我国可持续发展的重要保证.
Ⅰ.火力发电燃煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如下图所示:

(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释原因CO32-+H2O?HCO3-+OH-或HCO3-+H2O?H2CO3-+OH-.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是2H2SO3+O2═2H2SO4 中和、稀释经氧气氧化后海水中生成的酸.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH=2.O,ρ≈1g•mL-1)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol•L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
(3)你认为往废水中投入B (填字母序号),沉淀效果最好.
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=1.2×10-3mol/L.
(5)如果用食盐处理其只含Ag+的废水,测得处理后废水中NaCl的质量分数为0.117%.
若环境要求排放标准为c(Ag+)低于1.O×lO-8mol•L-1,问该工厂处理后的废水中c(Ag+)=9×10-9 mol/L.已知Ksp(AgCl)=1.8×l-10mol2•L2.
Ⅰ.火力发电燃煤排放的SO2会造成一系列环境和生态问题.利用海水脱硫是一种有效的方法,其工艺流程如下图所示:

(1)天然海水的pH≈8,呈弱碱性.用离子方程式解释原因CO32-+H2O?HCO3-+OH-或HCO3-+H2O?H2CO3-+OH-.
(2)天然海水吸收了含硫烟气后,要用O2进行氧化处理,氧化后的“海水”需要用大量的天然海水与之混合后才能排放,该操作的主要目的是2H2SO3+O2═2H2SO4 中和、稀释经氧气氧化后海水中生成的酸.
Ⅱ.重金属离子对河流及海洋造成严重污染.某化工厂废水(pH=2.O,ρ≈1g•mL-1)中含有Ag+、Pb2+等重金属离子,其浓度各约为0.01mol•L-1.排放前拟用沉淀法除去这两种离子,查找有关数据如下:
| 难溶电解质 | AgI | AgOH | Ag2S | PbI2 | Pb(OH)2 | PbS |
| Ksp | 8.3×10-17 | 5.6×10-8 | 6.3×10-50 | 7.1×10-9 | 1.2×10-15 | 3.4×10-28 |
A.NaOH B.Na2S C.KI D.Ca(OH)2
(4)如果用生石灰处理上述废水,使溶液的pH=8.0,处理后的废水中c(Pb2+)=1.2×10-3mol/L.
(5)如果用食盐处理其只含Ag+的废水,测得处理后废水中NaCl的质量分数为0.117%.
若环境要求排放标准为c(Ag+)低于1.O×lO-8mol•L-1,问该工厂处理后的废水中c(Ag+)=9×10-9 mol/L.已知Ksp(AgCl)=1.8×l-10mol2•L2.
20.下列物质属于非电解质的是( )
| A. | HNO3 | B. | Cu | C. | SO2 | D. | NH4NO3 |
19.(1)为达下表所列实验目的,请选择合适的实验方法,将其标号填在相应的空格中.
A、加热至恒重 B、用氢氧化钠溶液溶解后过滤
C.溶解、过滤、结晶 D.滴加KSCN溶液观察是否溶液是否变红
(2)实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液.为鉴别两溶液,进行以下实验:取甲溶液于试管,向其中缓慢滴入乙溶液,并边滴加边振荡,观察到开始无明显现象,后来有大量气体生成.甲是Na2CO3溶液;
实验过程中所发生反应的离子方程式为:CO32-+H+=HCO3-、HCO3-+H+=CO2+H2O;
(3)将CO2和SO2气体分别通入酸性高锰酸钾,使之褪色的是SO2气体,请写出该反应的离子方程式:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+.
| 实验目的 | 标号 |
| 检验氯化亚铁是否变质 | |
| 除去食盐中少量细砂 | |
| 除去碳酸钠固体中少量碳酸氢钠 | |
| 除去镁粉中混有的少量铝粉 |
C.溶解、过滤、结晶 D.滴加KSCN溶液观察是否溶液是否变红
(2)实验室有甲、乙两瓶无色溶液,其中一瓶是稀盐酸,另一瓶是碳酸钠溶液.为鉴别两溶液,进行以下实验:取甲溶液于试管,向其中缓慢滴入乙溶液,并边滴加边振荡,观察到开始无明显现象,后来有大量气体生成.甲是Na2CO3溶液;
实验过程中所发生反应的离子方程式为:CO32-+H+=HCO3-、HCO3-+H+=CO2+H2O;
(3)将CO2和SO2气体分别通入酸性高锰酸钾,使之褪色的是SO2气体,请写出该反应的离子方程式:5SO2+2MnO4-+2H2O=2Mn2++5SO42-+4H+.
17.NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 16g氧气所含的氧原子数为2NA | |
| B. | 18g水所含的电子数为NA | |
| C. | 2.4g金属镁与盐酸(足量)反应失去的电子数为0.1NA | |
| D. | 17g氨气所含电子数目为10NA |
16.下列说法正确的是( )
| A. | 18gD2O中含有的中子数为10 NA(设NA为阿伏加德罗常数的数值) | |
| B. | 电解精炼铜时,每转移1mol电子,阳极溶解铜的质量为32g | |
| C. | 恒温恒容下,某可逆反应X(g)+Y(g)?Z(g)+W(s)△H>0达平衡后再加入X,该反应的△H增大 | |
| D. | 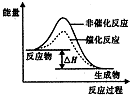 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
15.现有下列反应式,据两式判断,下列各组离子中,氧化性由强到弱的排列顺序正确的是
(1)2Fe3++2I-═2Fe2++I2 (2)Br2+2Fe2+═2Fe3++2Br-( )
0 153000 153008 153014 153018 153024 153026 153030 153036 153038 153044 153050 153054 153056 153060 153066 153068 153074 153078 153080 153084 153086 153090 153092 153094 153095 153096 153098 153099 153100 153102 153104 153108 153110 153114 153116 153120 153126 153128 153134 153138 153140 153144 153150 153156 153158 153164 153168 153170 153176 153180 153186 153194 203614
(1)2Fe3++2I-═2Fe2++I2 (2)Br2+2Fe2+═2Fe3++2Br-( )
| A. | Br2>Fe2+>I2 | B. | Br2>Fe3+>I2 | C. | I2>Br2>Fe3+ | D. | Fe3+>Br2>I2 |