题目内容
16.下列说法正确的是( )| A. | 18gD2O中含有的中子数为10 NA(设NA为阿伏加德罗常数的数值) | |
| B. | 电解精炼铜时,每转移1mol电子,阳极溶解铜的质量为32g | |
| C. | 恒温恒容下,某可逆反应X(g)+Y(g)?Z(g)+W(s)△H>0达平衡后再加入X,该反应的△H增大 | |
| D. | 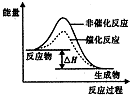 如图表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 |
分析 A、根据n=$\frac{m}{M}$计算物质的量结合重水分子式计算中子数;
B、电解精炼铜时,阳极上除了铜放电,还有比铜活泼的金属放电;
C、反应热△H与物质的化学计量数有关,与参加反应的物质的物质的量无关;
D、催化剂可以降低反应的活化能,从而加快化学反应的速率;
解答 解:A、一个D2O中含有1×2+8=10个中子,8gD2O物质的量=$\frac{18g}{20g/mol}$=0.9mol,含有10NA个中子,故A错误;
B、电解精炼铜时,阳极上除了铜放电,还有比铜活泼的金属放电,故当转移NA个电子时,阳极的质量减少小于32g,故B错误;
C、反应热△H与物质的化学计量数有关,物质的化学计量数不变,热化学方程式中反应热不变,与参加反应的物质的物质的量无关,故C错误;
D、反应物的总能量大于生成物的总能量,则反应是放热反应,加入催化剂会降低活化能,改变反应的速率,但反应热不改变,故D正确;
故选D.
点评 本题考查了物质的量的有关计算,铜的精炼,反应热的大小和催化剂的工作原理等,难度不大,把握概念是解题关键,难度不大.

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
6.化学与科学、技术、社会、环境密切相关,下列有关说法中错误的是( )
| A. | 大量排放NO和NO2等氮氧化物是形成光化学烟雾和酸雨的一个重要原因 | |
| B. | 采用纳米二氧化钛光触媒技术,将汽车尾气中的NO和CO转化为无害气体 | |
| C. | 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遭遇强碱会“断路” | |
| D. | 大量燃烧化石燃料排放的废气中含大量SO2,从而使雨水的pH=5.6,形成酸雨 |
7.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 25℃,pH=12的Na2CO3溶液中含有OH-的数目为0.01NA | |
| B. | 1 mol苯乙烯( )中含有的碳碳双键数为4NA )中含有的碳碳双键数为4NA | |
| C. | 加热条件下,4.6g金属Na与足量O2反应的产物中阳离子和阴离子总数为0.3NA | |
| D. | 常温时,1 L0.1 mol•L-1的硝酸铵溶液中,NH4+和H+总数为0.1NA |
4.下列化学用语正确的是( )
| A. | OH-的电子式: | |
| B. | 乙酸的分子式C2H4O2 | |
| C. | 硫离子结构示意图 | |
| D. | 氢氧化钡电离方程式:Ba(OH)2═Ba2++OH2- |
11.下列说法正确的是( )
| A. | 摩尔是物质质量的单位 | B. | 1 mol气体所占的体积一定是22.4L | ||
| C. | 1mol水质量为18g | D. | 氢气的摩尔质量是2g |
8.下列说法正确的是( )
| A. | CO2的比例模型为 | |
| B. | H2O2的电子式是H:O:O:H | |
| C. | 甲烷的结构式为CH4 | |
| D. | 熔融状态下NaHSO4的电离方程式为NaHSO4=Na++HSO4- |
5.下列反应的离子方程式书写正确的是( )
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | 稀 H2SO4与铁粉反应:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 钠放入水中:Na+H2O═Na++OH-+H2↑ | |
| D. | 氢氧化镁溶于盐酸:Mg(OH)2+2H+═Mg2++2H2O. |
6.工业上以粗盐为原料制取氢氧化钠时,首先要对粗盐进行除杂精制,为除去粗盐中的MgCl2、CaCl2、Na2SO4杂质,可加入氯化钡溶液、氢氧化钠溶液、碳酸钠溶液.则这三种试剂加入的顺序正确的是( )
| A. | 氢氧化钠溶液、碳酸钠溶液、氯化钡溶液 | |
| B. | 氢氧化钠溶液、氯化钡溶液、碳酸钠溶液 | |
| C. | 氯化钡溶液、碳酸钠溶液、氢氧化钠溶液 | |
| D. | 碳酸钠溶液、氯化钡溶液、氢氧化钠溶液 |