1.有些科学家提出硅是“21 世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用.下列关于硅及其化合物的说法正确的是( )
| A. | 水泥、玻璃、水晶饰物都是硅酸盐制品 | |
| B. | 高温下,可在试管内完成焦炭和石英砂(SiO2)制取硅的反应 | |
| C. | 光导纤维的主要成分是SiO2 | |
| D. | 自然界中硅元素的贮量丰富,并存在大量的单质硅 |
18.一定条件下,碳钢腐蚀与溶液pH的关系如下表.下列说法不正确的是( )
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
| 腐蚀快慢 | 较快 | 慢 | 较快 | ||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2- | |||
| A. | 当溶液pH<4,碳钢主要发生析氢腐蚀 | |
| B. | 当溶液pH>13.5,碳钢腐蚀的正极反应式为O2+4H++4e-=2H2O | |
| C. | 当溶液pH>6,碳钢主要发生吸氧腐蚀 | |
| D. | 煮沸除去氧气的碱性溶液中,碳钢腐蚀速率会减缓 |
17.化学反应中一定伴随着能量的变化,下列有关能量的说法正确的是( )
| A. | 等物质的量的硫蒸气和硫粉分别完全燃烧,后者放出热量多 | |
| B. | 由C(石墨)═C(金刚石)-1.9KJ可知,金刚石比石墨稳定 | |
| C. | 根据热化学方程式:S(s)+O2(g)═SO2(g)+297.23 kJ,可推知1 mol SO2 (g)的能量总和大于1 mo S(s)和1 mol O2(g)的能量总和 | |
| D. | 在稀水溶液中 H+(aq)+OH-(aq)═H2O(l)+57.3 kJ,将含0.5 mol H2SO4的浓硫酸与含l mol NaOH的溶液混合时,放出的热量大于57.3 kJ |
16.镁-空气电池的工作原理如图所示.下列说法不正确的是( )


| A. | 工作一段时间后,c(Na+)变大 | |
| B. | 电池工作时,OH-向a极移动 | |
| C. | 气体X 中N2的百分含量与空气相同 | |
| D. | 电池总反应为2Mg+O2+2H2O═2 Mg(OH)2 |
15.下列说法正确的是( )
| A. | 在100℃、101 kPa条件下,液态水的气化热为40.69 kJ•mol-1,则H2O(g)?H2O(l) 的△H=40.69 kJ•mol-1 | |||||||||||
| B. | Li、Be、B三种元素的第一电离能(I1)差别不大,而I2差别很大,则三种原子中最难失去第二个电子的是Be | |||||||||||
| C. | 已知:
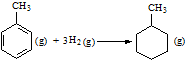 的△H为-384 kJ•mol-1 的△H为-384 kJ•mol-1 | |||||||||||
| D. | 固体NH5的所有原子的最外层均满足2个或8个电子的稳定结构,它与水反应的化学方程式为NH5+H2O═NH3•H2O+H2↑ |
14.已知:(1)Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s),△H=-348.3kJ/mol
(2)Zn(s)+Ag2O(s)═ZnO(s)+2Ag(s),△H=-317.3kJ/mol
则2Ag(s)+$\frac{1}{2}$O2(g)═Ag2O(s)的△H等于( )
0 152882 152890 152896 152900 152906 152908 152912 152918 152920 152926 152932 152936 152938 152942 152948 152950 152956 152960 152962 152966 152968 152972 152974 152976 152977 152978 152980 152981 152982 152984 152986 152990 152992 152996 152998 153002 153008 153010 153016 153020 153022 153026 153032 153038 153040 153046 153050 153052 153058 153062 153068 153076 203614
(2)Zn(s)+Ag2O(s)═ZnO(s)+2Ag(s),△H=-317.3kJ/mol
则2Ag(s)+$\frac{1}{2}$O2(g)═Ag2O(s)的△H等于( )
| A. | 31.0kJ/mol | B. | -665.6kJ/mol | C. | 332.8 kJ/mol | D. | -31.0 kJ/mol |
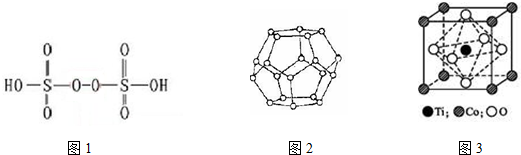
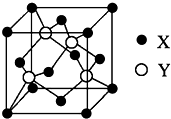 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题: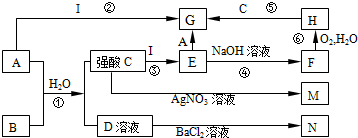
 ;
;