题目内容
14.已知:(1)Zn(s)+$\frac{1}{2}$O2(g)═ZnO(s),△H=-348.3kJ/mol(2)Zn(s)+Ag2O(s)═ZnO(s)+2Ag(s),△H=-317.3kJ/mol
则2Ag(s)+$\frac{1}{2}$O2(g)═Ag2O(s)的△H等于( )
| A. | 31.0kJ/mol | B. | -665.6kJ/mol | C. | 332.8 kJ/mol | D. | -31.0 kJ/mol |
分析 根据已知的热化学反应方程式和目标反应,利用盖斯定律来计算目标反应的反应热,以此来解答.
解答 解:由(1)Zn(s)+$\frac{1}{2}$O2(g)=ZnO(s)△△H=-348.3kJ/mol,
(2)Zn(s)+Ag2O(s)═ZnO(s)+2Ag(s),△H=-317.3kJ/mol
根据盖斯定律可知,(1)-(2)可得2Ag(s)+$\frac{1}{2}$O2(g)=Ag2O(s)
则△H=(-348.3kJ•mol-1)-(-317.3kJ•mol-1)=-31.0kJ•mol-1,
故选:D.
点评 本题考查学生利用盖斯定律计算反应的反应热,明确已知反应和目标反应的关系是解答本题的关键,难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.在FeCl2溶液加入过量Na2O2固体,充分搅拌(此时烧杯中液体呈浑浊状)后再加入过量盐酸使固体全部溶解,此时烧杯中阳离主要有( )
| A. | 只有Fe2+ | B. | Na+、Fe3+ | ||
| C. | Na+、Fe3+ 和H+ | D. | H+、Na+、Fe3+ 和Fe2+ |
5.下列说法不正确的是①将盛有二氧化氮气体的试管倒立在水中,溶液充满试管 ②酒精灯加热铝箔至熔化,铝并不滴落,说明铝表面生成了一层致密的氧化膜 ③向蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有吸水性( )
| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
2.下列说法不正确的是( )
| A. | 为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤 | |
| B. | 除去乙醇中的水:加入生石灰,蒸馏 | |
| C. | 为除去乙炔气中少量的H2S,可使其通过CuSO4溶液 | |
| D. | 为除去CO2中少量的SO2,可使其通过饱和Na2CO3溶液 |
3.下列离子方程式正确的是( )
| A. | 碳酸钙和盐酸反应:CO32-+2H+═H2O+CO2↑ | |
| B. | 向氢氧化钡溶液中加硫酸溶液:Ba2++SO42-═BaSO4↓ | |
| C. | 向稀盐酸溶液中加铁:3Fe+6H+═3Fe3++3H2↑ | |
| D. | 向硝酸银溶液中加盐酸:Ag++Cl-═AgCl↓ |
 针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动:
针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动: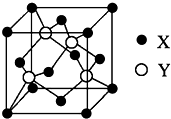 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题: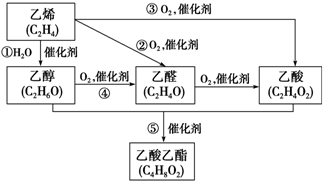 如图是由乙烯合成乙酸乙酯的几种可能的合成路线:
如图是由乙烯合成乙酸乙酯的几种可能的合成路线: