9.1774年,瑞典化学家舍勒把软锰矿(MnO2)与浓盐酸混合并加热,产生了一种黄绿色的气体,下列关于该气体的叙述正确的是( )
| A. | 该气体有毒、无味、密度比空气大 | |
| B. | 将该气体通入紫色石蕊溶液中,石蕊熔液先变红后褪色 | |
| C. | 该气体的性质活泼,它与氢气混合后立即发生爆炸 | |
| D. | 室温下该气体能用钢瓶贮运,所以该气体不与铁反应 |
8.下列离子方程式不正确的是( )
| A. | 向NaClO溶液中滴入少量FeSO4溶液:2Fe2++ClO-+2H+=Cl-+2Fe3++H2O | |
| B. | 氢氧化铁溶于氢碘酸中:2Fe(OH)3+6H++2I-=2Fe2++I2+3H2O | |
| C. | 碳酸氢钠溶液与少量澄清石灰水反应:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O | |
| D. | Na2SO3溶液中SO32-的水解:SO32-+H2O$\frac{\underline{\;电解\;}}{\;}$HSO3-+OH- |
6.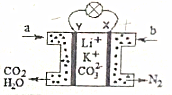 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH3OH为燃料时,该电池工作原理如图.下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH3OH为燃料时,该电池工作原理如图.下列说法正确的是( )
 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH3OH为燃料时,该电池工作原理如图.下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH3OH为燃料时,该电池工作原理如图.下列说法正确的是( )| A. | b为空气,电子由X极经导线流向Y极 | |
| B. | 在熔融电解质中,CO32-向X极移动 | |
| C. | 消耗1molCH3OH,消耗氧气分子数目约为3×6.02×1023 | |
| D. | 正极反应式为:O2+2CO2+4e-═2CO32- |
5.下列对实验现象的解释与结论正确的是( )
| A. | 向铜和稀硫酸的混合物中加入某无色溶液,溶液逐渐变成蓝色,铜逐渐溶解,则该无色溶液一定是硝酸 | |
| B. | 用蘸有浓氨水的玻璃棒置于某无机酸浓溶液的试剂瓶口,有大量白烟,说明该无机酸一定为盐酸 | |
| C. | SO2气体通入Ba(NO3)2溶液中,溶液出现浑浊现象,说明有BaSO3沉淀生成 | |
| D. | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡、静置,下层溶液显紫红色,说明Fe3+的氧化性大于I2 |
4.下列说法正确的是( )
| A. | SiO2(s)+2C(s)═Si(s)+2CO(g)只能在高温下自发进行,则该反应△H>0 | |
| B. | 室温下,pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液pH>7 | |
| C. | 合成氨生产中将NH3液化分离,一定能加快正反应速率,提高H2的转化率 | |
| D. | 25℃时,向0.1mol•L-1CH3COOH溶液滴加氨水,c(H+)/c(CH3COOH)增大 |
3.下列说法的是( )
| A. | 金刚石晶体中的最小碳原子环由6个碳原子构成 | |
| B. | SO3晶体属于原子晶体 | |
| C. | 1molSiO2晶体中含有2molSi-O键 | |
| D. | 金刚石化学性质稳定,即使高温下也不会和O2反应 |
1.将一块光洁的铁片放入100mL某浓度的硝酸中,当反应不再有气体放出时,取出铁片洗净晾干称重,发现铁片质量减少了4.2g.则该硝酸的浓为( )
| A. | 1.5mol/L | B. | 3.0mol/L | C. | 2.0mol/L | D. | 无法计算 |
20.浓度均为0.1mol•L-1的三种溶液等体积混合,充分反应后没有沉淀的一组溶液是( )
0 152728 152736 152742 152746 152752 152754 152758 152764 152766 152772 152778 152782 152784 152788 152794 152796 152802 152806 152808 152812 152814 152818 152820 152822 152823 152824 152826 152827 152828 152830 152832 152836 152838 152842 152844 152848 152854 152856 152862 152866 152868 152872 152878 152884 152886 152892 152896 152898 152904 152908 152914 152922 203614
| A. | BaCl2,NaOH,NaHCO3 | B. | Na2CO3,MgCl2,H2SO4 | ||
| C. | AgNO3,HCl,NaOH | D. | Ba(OH)2,CaCl2,Na2SO4 |
 在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图所示.
在容积为VL的密闭容器中发生2NO2?2NO+O2反应.反应过程中NO2的物质的量随时间变化的状况如图所示.