题目内容
6.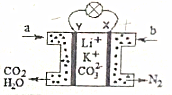 某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH3OH为燃料时,该电池工作原理如图.下列说法正确的是( )
某种熔融碳酸盐燃料电池以Li2CO3、K2CO3为电解质、以CH3OH为燃料时,该电池工作原理如图.下列说法正确的是( )| A. | b为空气,电子由X极经导线流向Y极 | |
| B. | 在熔融电解质中,CO32-向X极移动 | |
| C. | 消耗1molCH3OH,消耗氧气分子数目约为3×6.02×1023 | |
| D. | 正极反应式为:O2+2CO2+4e-═2CO32- |
分析 该原电池为甲烷燃料电池,根据图象可知a极生成二氧化碳和水,则应为甲醇被氧化生成,则左边电极为负极、右边电极为之间,所以a为CH3OH、b为空气,负极反应式为CH3OH+3CO32--6e-=4CO2+2H2O,正极反应式为O2+2CO2+4e-═2CO32-,以此解答该题.
解答 解:A.b为空气,则b为正极,Y为负极,电子由Y极经导线流向X极,故A错误;
B.原电池工作时,阴离子向负极移动,故B错误;
C.负极反应式为CH3OH+3CO32--6e-=4CO2+2H2O,正极反应式为O2+2CO2+4e-═2CO32-,消耗1molCH3OH,则转移6mol电子,应消耗1.5mol氧气,故C错误;
D.正极发生还原反应,电极反应式为O2+2CO2+4e-═2CO32-,故D正确.
故选D.
点评 本题考查了化学电源新型电池,明确原电池中物质得失电子、电子流向、离子流向即可解答,难点是电极反应式书写,要根据电解质确定正负极产物,难度中等.

练习册系列答案
相关题目
17.用NA代表阿伏加德罗常数的值,下列有关说法正确的是( )
| A. | 1 mol 过氧化钠与水反应时转移电子数为2NA | |
| B. | 16g氧气中所含的电子数为NA | |
| C. | 22.4L氯化氢溶于水可电离出1mol Cl- | |
| D. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
14.A、B为短周期元素,它们的原子的最外层电子数相同,且A的原子半径小于B,若m为正整数,则下列说法正确的是( )
| A. | 若HnAOm是强酸,则HnBOm也一定为强酸 | |
| B. | 若一定条件下,金属A的单质能与水反应,则B的单质也一定能与水反应 | |
| C. | 常温下,若B的氢化物是气体,则A的氢化物也一定是气体 | |
| D. | A的单质可能从B的化合物中置换出B |
1.将一块光洁的铁片放入100mL某浓度的硝酸中,当反应不再有气体放出时,取出铁片洗净晾干称重,发现铁片质量减少了4.2g.则该硝酸的浓为( )
| A. | 1.5mol/L | B. | 3.0mol/L | C. | 2.0mol/L | D. | 无法计算 |
2.下列有关叙述错误的是( )
| A. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| B. | 陶瓷、水泥和光导纤维均属于硅酸盐材料 | |
| C. | “煤改气”、“煤改电”等清洁燃料改造工程有利于减少雾霾天气 | |
| D. | 石油裂解、煤的干馏、玉米制醇、蛋白质的变性都是化学变化 |
19.A、B、C、D四种可溶性物质,都是由下表中的离子形成的.
已知每种物质中阴阳离子互不重复.
①若把四种物质分别溶解于盛有蒸馏水的四支试管中,只有C溶液呈蓝色.
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味的气体逸出.
(1)根据①②实验事实可推断它们的化学式为:
ABa(OH)2,BAgNO3,CCuSO4,DNa2CO3.
(2)写出下列反应的离子方程式:
a.A溶液与C溶液混合:Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓
b.向A溶液中加入NaHSO4溶液至Ba2+恰好沉淀完全:Ba2++SO42-+OH-+H+=H2O+BaSO4↓.
| 阳离子 | Ba2+ | Ag+ | Na+ | Cu2+ |
| 阴离子 | NO3- | SO42- | OH- | CO32- |
①若把四种物质分别溶解于盛有蒸馏水的四支试管中,只有C溶液呈蓝色.
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味的气体逸出.
(1)根据①②实验事实可推断它们的化学式为:
ABa(OH)2,BAgNO3,CCuSO4,DNa2CO3.
(2)写出下列反应的离子方程式:
a.A溶液与C溶液混合:Cu2++2OH-+Ba2++SO42-=BaSO4↓+Cu(OH)2↓
b.向A溶液中加入NaHSO4溶液至Ba2+恰好沉淀完全:Ba2++SO42-+OH-+H+=H2O+BaSO4↓.
20.下列有关化学实验安全问题的叙述中不正确的是( )
| A. | 闻化学药品的气味时都不能使鼻子凑近药品 | |
| B. | 点燃氢气前要检查纯度,以免发生爆炸 | |
| C. | 在盛O2集气瓶中进行铁丝燃烧实验时,事先在集气瓶底铺上一层沙子 | |
| D. | 凡是给玻璃仪器加热,都要加垫石棉网,以防仪器炸裂 |
 CH3COO-+H+醋酸的电离平衡常数表达式K=$\frac{[C{H}_{3}COO{\;}^{-}][H{\;}^{+}]}{[C{H}_{3}COOH]}$,达平衡时溶液中氢离子的浓度4×10-4mol/L(25℃,醋酸的电离常数为1.6×10-5;醋酸的电离程度很小,可近似认为醋酸的浓度不变).
CH3COO-+H+醋酸的电离平衡常数表达式K=$\frac{[C{H}_{3}COO{\;}^{-}][H{\;}^{+}]}{[C{H}_{3}COOH]}$,达平衡时溶液中氢离子的浓度4×10-4mol/L(25℃,醋酸的电离常数为1.6×10-5;醋酸的电离程度很小,可近似认为醋酸的浓度不变).