13.下列有机物命名正确的是( )
| A. |  3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | |
| B. |  2-羟基丁烷 2-羟基丁烷 | |
| C. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | |
| D. | CH3CH(CH3)CH2COOH 3-甲基丁酸 |
11.已知:①N2(g)+O2(g)═2NO(g)△H1=+180kJ•mol-1
②N2(g)+3H2 (g)?2NH3 (g)△H2=-92.4kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H3=-483.6kJ•mol-1
下列说法正确的是( )
②N2(g)+3H2 (g)?2NH3 (g)△H2=-92.4kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H3=-483.6kJ•mol-1
下列说法正确的是( )
| A. | 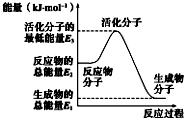 反应②中的能量变化如图所示,则△H2=E1-E3 | |
| B. | N2的燃烧热为180kJ•mol-1 | |
| C. | 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和 3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和 6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 | |
| D. | 氨的催化氧化反应为 4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=+906 kJ•mol-1 |
9. 已知制备甲醇的有关化学反应及平衡常数如表所示:
已知制备甲醇的有关化学反应及平衡常数如表所示:
(1)则反应△H3=-90kJ•molˉ1;K2=0.5(填数据);
(2)850℃时,在密闭容器中进行反应①,开始时只加入CO2、H2,反应10min后测得各组分的浓度如下
(Ⅰ)该时间段内反应速率v(H2)=0.12mol/(L•min);
(Ⅱ)比较此时正逆反应的速率的大小:v正>v逆(选填“>、<或=”);
(Ⅲ)反应达到平衡后,保持其他条件不变,只把容器的体积缩小一半,平衡正向(选填“逆向”、“正向”或“不”)移动,该反应的平衡常数不变(选填“增大”“减小”“不变”).
(3)依据温度对反应①的影响,在图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,甲醇物质的量变化的曲线示意图.
 已知制备甲醇的有关化学反应及平衡常数如表所示:
已知制备甲醇的有关化学反应及平衡常数如表所示:| 化学反应 | 反应热 | 平衡常数(850℃) |
| ①CO2 (g)+3H2 (g)═CH3OH(g)+H2O(g) | △H1=-48.8 kJ•molˉ1 | K1=320 |
| ②CO(g)+H2O(g)═H2(g)+CO2(g) | △H2=-41.2 kJ•molˉ1 | K2 |
| ③CO(g)+2H2(g)═CH3OH(g) | △H3 | K3=160 |
(2)850℃时,在密闭容器中进行反应①,开始时只加入CO2、H2,反应10min后测得各组分的浓度如下
| 物质 | H2 | CO2 | CH3OH | H2O |
| 浓度(mol•Lˉ1) | 0.2 | 0.2 | 0.4 | 0.4 |
(Ⅱ)比较此时正逆反应的速率的大小:v正>v逆(选填“>、<或=”);
(Ⅲ)反应达到平衡后,保持其他条件不变,只把容器的体积缩小一半,平衡正向(选填“逆向”、“正向”或“不”)移动,该反应的平衡常数不变(选填“增大”“减小”“不变”).
(3)依据温度对反应①的影响,在图坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,甲醇物质的量变化的曲线示意图.
8.下列四个图象的有关描述错误的是( )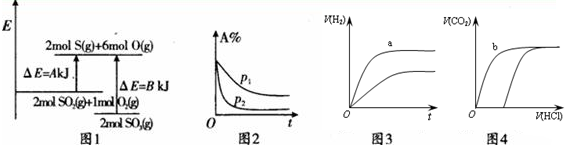
注:△E:表示能量,p表示压强;t表示时间,V表示体积,%表示B的体积百分含量.

注:△E:表示能量,p表示压强;t表示时间,V表示体积,%表示B的体积百分含量.
| A. | 图1表示化学反应2S02(g)+O2(g)?2S03(g)的能量变化,该反应的△H=A一BkJ/mol | |
| B. | 图2表示其他条件不变时,反应2A(g)+B(g)?c(g)+D(g)在不同压强下随时间的变化 | |
| C. | 图3表示体积和浓度均相同的HCl和CH3COOH两种溶液中,分别加入足量的锌,产生H2的体积随时间的变化,则a表示CH3COOH溶液 | |
| D. | 图4表示100 ml O.1 mol•L-Na2C03和NaHC03两种溶液中,分别逐滴滴加0.1 mol•L-1HCl,产生CO2 的体积随盐酸体积的变化,则b表示NaHCO3溶液 |
7.在N2+3H2═2NH3反应中,经过一段时间后,NH3的浓度增加了0.6mol/L,在此时间内,H2表示的平均反应速率为0.45mol/(L•S).所经过的时间是( )
| A. | 0.44s | B. | 1s | C. | 7.33s | D. | 2s |
6.已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.32kJ•mol-1,在容器中充入2mol SO2和1mol O2,充分反应,最终放出的热量( )
| A. | =196.64kJ | B. | =98.32kJ | C. | <196.64kJ | D. | >196.64kJ |
5.在绝热情况下向四份0.1mol/L的醋酸钠溶液中分别加入少量KNO3固体、硫酸氢钾固体、氯化钠固体和硫酸铜粉末(忽略溶液体积变化),则c(Ac-)/c(Na+)的变化正确的是( )
0 152615 152623 152629 152633 152639 152641 152645 152651 152653 152659 152665 152669 152671 152675 152681 152683 152689 152693 152695 152699 152701 152705 152707 152709 152710 152711 152713 152714 152715 152717 152719 152723 152725 152729 152731 152735 152741 152743 152749 152753 152755 152759 152765 152771 152773 152779 152783 152785 152791 152795 152801 152809 203614
| A. | 增大、增大、不变、减小 | B. | 减小、增大、不变、减小 | ||
| C. | 增大、减小、减小、减小 | D. | 增大、减小、减小、增大 |