题目内容
11.已知:①N2(g)+O2(g)═2NO(g)△H1=+180kJ•mol-1②N2(g)+3H2 (g)?2NH3 (g)△H2=-92.4kJ•mol-1
③2H2(g)+O2(g)═2H2O(g)△H3=-483.6kJ•mol-1
下列说法正确的是( )
| A. | 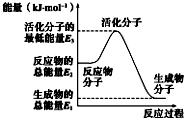 反应②中的能量变化如图所示,则△H2=E1-E3 | |
| B. | N2的燃烧热为180kJ•mol-1 | |
| C. | 由反应②知在温度一定的条件下,在一恒容密闭容器中通入1 mol N2和 3 mol H2,反应后放出的热量为Q1 kJ,若通入2 mol N2和 6 mol H2反应后放出的热量为Q2 kJ,则184.8>Q2>2Q1 | |
| D. | 氨的催化氧化反应为 4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=+906 kJ•mol-1 |
分析 A、反应热等于生成物的总能量-反应物的总能量;
B、燃烧热是1mol可燃物完全燃烧是稳定氧化物放出的热量,氮气和氧气生成的一氧化氮不是稳定氧化物,会和氧气反应生成二氧化氮;
C、合成氨的反应为可逆反应,压强增大平衡向正反应方向移动,92.4kJ•mol-1为生成2mol氨气时放出的热量;
D、由已知热化学方程式根据盖斯定律构造目标热化学方程式.
解答 解:A、反应热等于生成物的总能量-反应物的总能量,因此△H2=E1-E2,故A错误;
B、燃烧热是1mol可燃物完全燃烧是稳定氧化物放出的热量,氮气和氧气生成的一氧化氮不是稳定氧化物,会和氧气反应生成二氧化氮,N2(g)+O2(g)═2NO(g)△H1=+180kJ•mol-1不符合燃烧热概念,故B错误;
C、合成氨的反应为可逆反应,压强增大平衡向正反应方向移动,因此Q2>2Q1,92.4kJ•mol-1为生成2mol氨气时放出的热量,可逆反应不能进行到底,因此92.4×2>Q2,则184.8>Q2>2Q1,故C正确;
D、已知:①N2(g)+O2(g)=2NO(g)△H=+180kJ/mol
②N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ/mol
③2H2(g)+O2(g)=2H2O(g)△H=-483.6kJ/mol
由盖斯定律可知,①×2-②×2+③×3得:4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H=-906kJ/mol,故D错误;
故选C.
点评 本题考查反应热和焓变的计算以及化学平衡移动对反应热的影响,难度中等,其中C为本题的难点,综合性较强.

练习册系列答案
相关题目
6.已知热化学方程式:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98.32kJ•mol-1,在容器中充入2mol SO2和1mol O2,充分反应,最终放出的热量( )
| A. | =196.64kJ | B. | =98.32kJ | C. | <196.64kJ | D. | >196.64kJ |
3.某化学活动小组按下图所示流程由粗氧化铜样品(含少量氧化亚铁及不溶于酸的杂质)制取无水硫酸铜.
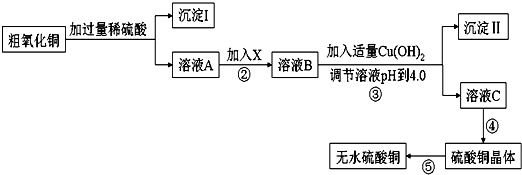
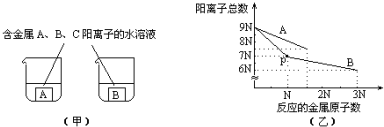
已知Fe3+、Cu2+、Fe2+三种离子在水溶液中形成氢氧化物沉淀的pH范围如下图所示:
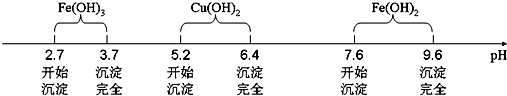
请回答下列问题:
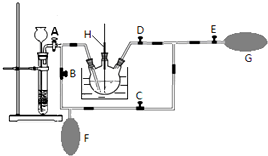
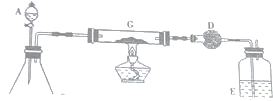
(1)在整个实验过程中,下列实验装置不可能用到的是①③(填序号)
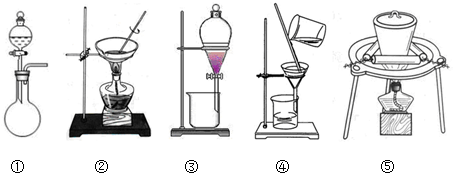
(2)溶液A中所含溶质为CuSO4、FeSO4、H2SO4;
(3)物质X应选用②(填序号),沉淀Ⅱ的主要成分是Fe(OH)3
①氯水 ②双氧水 ③铁粉 ④高锰酸钾
(4)从溶液C中制取硫酸铜晶体的实验操作为蒸发浓缩、冷却结晶、过滤、自然干燥.
(5)用“间接碘量法”可以测定溶液A中Cu2+(不含能与I-发生反应的杂质)的浓度.过程如下:
第一步:移取10.00mL溶液A于100mL容量瓶,加水定容至100mL.
第二步:取稀释后试液20.00mL于锥形瓶中,加入过量KI固体,充分反应生成白色沉淀与碘单质.
第三步:以淀粉溶液为指示剂,用0.05000mol•L-1的Na2S2O3标准溶液滴定,前后共测定三组.达到滴定终点时,消耗Na2S2O3标准溶液的体积如下表:
(已知:I2+2S2O32-═2I-+S4O62-)
①CuSO4溶液与KI的反应的离子方程式为2Cu2++4I-═2CuI↓+I2.
②滴定中,试液Na2S2O3应放在碱式滴定管(填“酸式滴定管”或“碱式滴定管”),判断滴定终点的依据是最后一滴试液滴入,溶液由蓝色变为无色,振荡半分钟,溶液无明显变化.
③溶液A中c(Cu2+)=0.5000mol•L-1.

已知Fe3+、Cu2+、Fe2+三种离子在水溶液中形成氢氧化物沉淀的pH范围如下图所示:

请回答下列问题:
(1)在整个实验过程中,下列实验装置不可能用到的是①③(填序号)

(2)溶液A中所含溶质为CuSO4、FeSO4、H2SO4;
(3)物质X应选用②(填序号),沉淀Ⅱ的主要成分是Fe(OH)3
①氯水 ②双氧水 ③铁粉 ④高锰酸钾
(4)从溶液C中制取硫酸铜晶体的实验操作为蒸发浓缩、冷却结晶、过滤、自然干燥.
(5)用“间接碘量法”可以测定溶液A中Cu2+(不含能与I-发生反应的杂质)的浓度.过程如下:
第一步:移取10.00mL溶液A于100mL容量瓶,加水定容至100mL.
第二步:取稀释后试液20.00mL于锥形瓶中,加入过量KI固体,充分反应生成白色沉淀与碘单质.
第三步:以淀粉溶液为指示剂,用0.05000mol•L-1的Na2S2O3标准溶液滴定,前后共测定三组.达到滴定终点时,消耗Na2S2O3标准溶液的体积如下表:
(已知:I2+2S2O32-═2I-+S4O62-)
| 滴定次数 | 第一次 | 第二次 | 第三次 |
| 滴定前读数(mL) | 0.10 | 0.36 | 1.10 |
| 滴定滴定后读数(mL) | 20.12 | 20.34 | 22.12 |
②滴定中,试液Na2S2O3应放在碱式滴定管(填“酸式滴定管”或“碱式滴定管”),判断滴定终点的依据是最后一滴试液滴入,溶液由蓝色变为无色,振荡半分钟,溶液无明显变化.
③溶液A中c(Cu2+)=0.5000mol•L-1.
20.下列物质属于酸的是( )
| A. | NaCl | B. | CO2 | C. | H2SO4 | D. | H2O |
1.在实验室里,下列溶液需用带橡胶塞的玻璃试剂瓶盛装的是( )
| A. | 氢氧化钠溶液 | B. | 浓盐酸 | C. | 浓硫酸 | D. | 氯化钠溶液 |
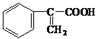 )和甲醇反应制得.
)和甲醇反应制得.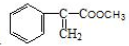
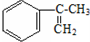 经过四步不同类型的反应制得阿托酸.
经过四步不同类型的反应制得阿托酸.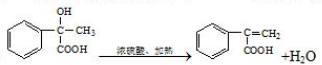 .
.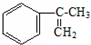 多两个碳原子的一种同系物,且A的所有碳原子可以处于同一平面上.写出A的结构简式
多两个碳原子的一种同系物,且A的所有碳原子可以处于同一平面上.写出A的结构简式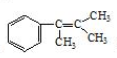 .
.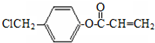 是阿托酸甲酯的某种同分异构体的一氯代物,其与足量氢氧化钠溶液共热,生成的有机产物的结构简式为
是阿托酸甲酯的某种同分异构体的一氯代物,其与足量氢氧化钠溶液共热,生成的有机产物的结构简式为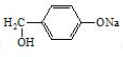 、
、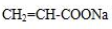 .
.