2.在某恒定温度下,向容积为2L的容器中投入1molSO2和2molNO2,发生如下反应:SO2(g)+NO2(g)?SO3(g)+NO(g),平衡时SO2的物质的量为$\frac{1}{3}$mol,若保持温度和容积不变,向其中增加2molNO2(g),使反应到达新的平衡,下列说法不正确的是( )
| A. | 新平衡时SO2的浓度是0.1mol•L-1 | |
| B. | 新平衡时NO2的转化率为20% | |
| C. | 新、旧平衡时容器内混合气体的平均相对分子质量之比为5:3 | |
| D. | 新、旧平衡时容器内气体的压强之比是5:3 |
20.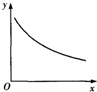 在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
 在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )
在某密闭容器中充入H2S和O2,发生反应:2H2S(g)+O2(g)?S2(g)+2H2O(g)△H<0,达到平衡后,若仅改变横坐标x的值,重新达到平衡后,纵坐标y随x变化趋势符合图象的是( )| 选项 | x | y |
| A | 温度 | 混合气体平均相对分子质量 |
| B | 压强 | S2气体体积分数 |
| C | 容器体积 | H2S浓度 |
| D | O2浓度 | 平常常数逆反应速率 |
| A. | A | B. | B | C. | C | D. | D |
19.设NA代表阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,11.2L的O2和NO的混合物含有的分子数约为0.5×6.02×1023 | |
| B. | 1mol的羟基与1 mol的氢氧根离子所含电子数均为9 NA | |
| C. | 常温常压下42g 乙烯和丁烯混合气体中,碳氢键的数目为6NA | |
| D. | 6.4g SO2与3.2g氧气反应生成SO3,转移电子数为0.2NA |
18.下列说法正确的是( )
| A. | 氧化还原反应的本质是化合价生了变化 | |
| B. | 化合价升高的物质被氧化 | |
| C. | 得到电子的物质被氧化 | |
| D. | 氧化还原反应中,先有氧化后有还原 |
16.能说明0.1mol•L-1的NaHA溶液一定呈酸性的是( )
①稀释时,溶液中c(OH-)增大
②溶液的pH<7
③溶液中c(Na+)=c(A2-)
④溶液可与等体积等物质的量浓度的NaOH溶液恰好反应.
①稀释时,溶液中c(OH-)增大
②溶液的pH<7
③溶液中c(Na+)=c(A2-)
④溶液可与等体积等物质的量浓度的NaOH溶液恰好反应.
| A. | ①②③④ | B. | ①③④ | C. | ①③ | D. | ②④ |
15.短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族.下列叙述正确的是( )
0 152466 152474 152480 152484 152490 152492 152496 152502 152504 152510 152516 152520 152522 152526 152532 152534 152540 152544 152546 152550 152552 152556 152558 152560 152561 152562 152564 152565 152566 152568 152570 152574 152576 152580 152582 152586 152592 152594 152600 152604 152606 152610 152616 152622 152624 152630 152634 152636 152642 152646 152652 152660 203614
| A. | 元素W的氢化物的稳定性比X的氢化物稳定性强 | |
| B. | 元素Y的最高价氧化物对应水化物为强碱 | |
| C. | 化合物YX、ZX2、WX2中化学键类型相同 | |
| D. | 原子半径的大小顺序:rY>rZ>rW>rX |
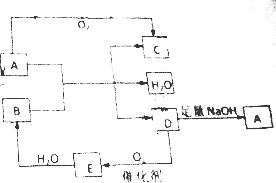 A、B、C、D、E五种物质都含有同一种元素,其中D在常温下为无色有刺激性气味的有毒气体,在一定条件下有如图所示的转化关系.
A、B、C、D、E五种物质都含有同一种元素,其中D在常温下为无色有刺激性气味的有毒气体,在一定条件下有如图所示的转化关系. ;
; 在稀硫酸、纯碱、二氧化碳、铜片、食盐、生石灰、三氧化钨、铁片和木炭粉9种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应.
在稀硫酸、纯碱、二氧化碳、铜片、食盐、生石灰、三氧化钨、铁片和木炭粉9种物质中,存在下面的相互关系,选择①~⑤为适当的物质,使有连线的两种物质能发生反应.