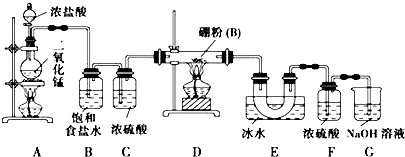
4.氯化铁是常见的水处理剂,工业上制备无水FeCl3的一种工艺如下:
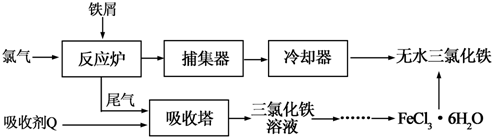
(1)试写出吸收塔中吸收剂Q反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-.
(2)六水合氯化铁在水中的溶解度如下:
从FeCl3溶液制得FeCl3•6H2O晶体的操作步骤是:加入少量盐酸、加热浓缩;、冷却结晶、过滤、洗涤、干燥.再由FeCl3•6H2O晶体得到无水FeCl3的操作是:在氯化氢气流中加热FeCl3•6H2O晶体,得到无水FeCl3.
(3)常温下,若溶液的pH控制不当会使Fe3+沉淀,pH=4时,溶液中c(Fe3+)=4×10-8mol•L-1.(常温下Ksp[Fe(OH)3]=4×10-38).
(4)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式SO2+2H2O+2Fe3+=2Fe2++4H++SO42-.
(5)向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式Fe(OH)3.请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释Fe3+会水解产生较多的H+:Fe3++3H2O?Fe(OH)3+3H+,加入CuO与H+反应生成Cu2+和H2O,降低了H+浓度,使得水解平衡正向移动,生成Fe(OH)3沉淀.

(1)试写出吸收塔中吸收剂Q反应的离子方程式:2Fe2++Cl2=2Fe3++2Cl-.
(2)六水合氯化铁在水中的溶解度如下:
| 温度/℃ | 0 | 10 | 20 | 30 | 50 | 80 | 100 |
| 溶解度(g/100gH2O) | 74.4 | 81.9 | 91.8 | 106.8 | 315.1 | 525.8 | 535.7 |
(3)常温下,若溶液的pH控制不当会使Fe3+沉淀,pH=4时,溶液中c(Fe3+)=4×10-8mol•L-1.(常温下Ksp[Fe(OH)3]=4×10-38).
(4)氯化铁溶液称为化学试剂中的“多面手”,写出SO2通入氯化铁溶液中反应的离子方程式SO2+2H2O+2Fe3+=2Fe2++4H++SO42-.
(5)向氯化铜和氯化铁的混合溶液中加入氧化铜粉末会产生新的沉淀,写出该沉淀的化学式Fe(OH)3.请用平衡移动的原理,结合必要的离子方程式,对此现象作出解释Fe3+会水解产生较多的H+:Fe3++3H2O?Fe(OH)3+3H+,加入CuO与H+反应生成Cu2+和H2O,降低了H+浓度,使得水解平衡正向移动,生成Fe(OH)3沉淀.
3.W、X、Y、Z均为短周期主族元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18.下列说法正确的是( )
| A. | 阴离子的半径:Z>Y | |
| B. | 气态氢化物稳定性:Z>Y>X | |
| C. | 氧化物的水化物的酸性:Z>Y | |
| D. | 元素W、X、Z各自最高和最低化合价的代数和分别为0、2、6 |
2.室温下,下列电解质溶液叙述正确的是( )
| A. | 25℃时若1 mL pH=1的盐酸与100 mL 氨水溶液混合后,溶液的pH=7,则氨水溶液的pH=11 | |
| B. | 将0.2 mol•L-1盐酸与0.1 mol•L-1的KAlO2溶液等体积混合,溶液中离子浓度由小到大的顺序:c(OH-)<c(H+)<c(Al3+)<c(K+)<c(Cl-) | |
| C. | pH相等的①NH4Cl ②(NH4)2SO4 ③NH4HSO4溶液:c(NH4+)大小顺序为②>①>③ | |
| D. | 0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) |
1.下列叙述正确的是( )
| A. | NaHCO3溶液中含有少量Na2CO3,可以用澄清石灰水除去 | |
| B. | 新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 | |
| C. | 加水稀释CH3COONa溶液,溶液中的所有离子浓度都减小 | |
| D. | 金属铝的生产是以Al2O3为原料,在熔融状态下进行电解 |
20.设NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA | |
| B. | 一定温度下,1 L 0.50 mol•L-1 NH4NO3溶液中含氮原子个数为NA | |
| C. | 过氧化氢分解制得1.12 L O2,转移电子数目为 0.2 NA | |
| D. | 235g核素${\;}_{92}^{235}$U发生裂变反应:${\;}_{92}^{235}$U+${\;}_{0}^{1}$n$\stackrel{裂变}{→}$${\;}_{38}^{90}$Sr+${\;}_{54}^{136}$Xe+10${\;}_{0}^{1}$n,净产生的中子(${\;}_{0}^{1}$n)数为10NA |
19.化学与生产、生活、社会密切相关.下列有关说法中正确的是( )
0 152415 152423 152429 152433 152439 152441 152445 152451 152453 152459 152465 152469 152471 152475 152481 152483 152489 152493 152495 152499 152501 152505 152507 152509 152510 152511 152513 152514 152515 152517 152519 152523 152525 152529 152531 152535 152541 152543 152549 152553 152555 152559 152565 152571 152573 152579 152583 152585 152591 152595 152601 152609 203614
| A. | 在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因 | |
| B. | 明矾水解时产生具有吸附性的胶体粒子,可以用于饮用水的杀菌消毒 | |
| C. | SO2具有漂白性,可用于漂白纸浆,也可以用于漂白食品 | |
| D. | 纯碱可用于生产普通玻璃,日常生活中也可用纯碱溶液来除去物品表面的油污 |
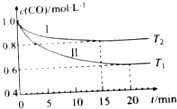 为了减少CO对大气的污染,某科研小组在一个体积为1L的容积不变的密闭容器中充入等量的CO和H2O(g),研究用CO和H2O(g)反应转化为绿色能源H2,不同温度下,CO的浓度[c(CO)]随时间[t]变化的曲线如图所示.
为了减少CO对大气的污染,某科研小组在一个体积为1L的容积不变的密闭容器中充入等量的CO和H2O(g),研究用CO和H2O(g)反应转化为绿色能源H2,不同温度下,CO的浓度[c(CO)]随时间[t]变化的曲线如图所示.