5.能说明Cl的非金属性比S强的事实有( )
①常温下S为固体,而Cl2为气体
②Cl2与H2混合,强光照射剧烈反应,而S与H2反应需较高温度
③与Fe反应,Cl2生成FeCl3,而S生成FeS
④盐酸是强酸,而氢硫酸是弱酸
⑤将Cl2通入氢硫酸中可置换出S.
①常温下S为固体,而Cl2为气体
②Cl2与H2混合,强光照射剧烈反应,而S与H2反应需较高温度
③与Fe反应,Cl2生成FeCl3,而S生成FeS
④盐酸是强酸,而氢硫酸是弱酸
⑤将Cl2通入氢硫酸中可置换出S.
| A. | ①③⑤ | B. | ②③⑤ | C. | ②③④ | D. | ②③④⑤ |
4.关于如图所示的原电池,下列说法正确的是( )


| A. | 锌电极发生还原反应:铜电极发生氧化反应 | |
| B. | 铜电极做正极发生的电极反应为:2H++2e-═H2↑ | |
| C. | 当有13g Zn溶解时,电路中就有0.5mol电子通过 | |
| D. | 电子从锌电极通过电流表流向铜电极 |
3.下列对化学用语的理解正确的是( )
| A. | 原子结构示意图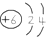 ,可以表示12C原子或13C原子 ,可以表示12C原子或13C原子 | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | 电子式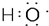 可以表示羟基或氢氧根离子 可以表示羟基或氢氧根离子 | |
| D. | CO2的比例模型: |
2.元素性质呈周期性变化的根本原因是( )
| A. | 元素相对原子质量依次递增 | |
| B. | 元素的最高正化合价呈周期性变化 | |
| C. | 元素原子最外层电子排布呈周期性变化 | |
| D. | 元素金属性或非金属性呈周期性变化 |
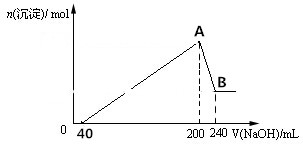
1.有一无色溶液,含有K+、Al3+、Mg2+、NH4+、Cl-、NO3-、HCO${\;}_{3}^{-}$、MnO4-中的几种.为确定其成分,做如下实验:①取部分溶液,加入7.8gNa2O2固体,产生无色的气体3.36L(STP)和白色沉淀,再加入1mol•L-1NaOH溶液300mL后白色沉淀全部溶解;②另取部分溶液,加入HNO3酸化的AgNO3溶液,产生28.7g白色沉淀.下列推断正确的是( )
| A. | 肯定有Al3+、Mg2+、NO3-,可能有NH4+、K+ | |
| B. | 肯定有Al3+、K+、Cl-,肯定没有MnO4-、Mg2+ | |
| C. | 肯定有Al3+、NH4+、Cl-、NO3-,一定没有HCO3-、Mg2+、MnO4- | |
| D. | 该溶液可能显弱酸性,也可能显中性 |
3.常温下,将CO2缓慢通入一定体积的NaOH溶液中,溶液的pH随通入CO2(标准状况)的变化曲线如图所示(忽略CO2的溶解),则下列说法中正确的是( )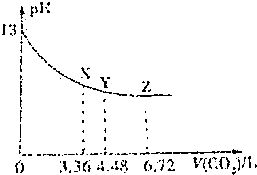

| A. | 该NaOH溶液的浓度为0.1mol/L,体积为6L | |
| B. | X、Y、Z三点对应的溶液中离子的种类不同 | |
| C. | Y点对应的融资中离子浓度关系为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+) | |
| D. | Y点对应的溶液中存在着:c(Na+)=2c(HCO3-)+c(OH-) |
1.一定温度下,在固定体积的密闭容器中进行可逆反应:N2+3H2?2NH3.该反应达到平衡的标志是( )
| A. | 3v(H2)正=2v(NH3)逆 | B. | 容器内的总压强不再随时间而变化 | ||
| C. | N2、H2、NH3的分子数之比为1:3:2 | D. | 混合气体的密度不再随时间变化 |
19.下列实验操作不会引起误差的是( )
0 152411 152419 152425 152429 152435 152437 152441 152447 152449 152455 152461 152465 152467 152471 152477 152479 152485 152489 152491 152495 152497 152501 152503 152505 152506 152507 152509 152510 152511 152513 152515 152519 152521 152525 152527 152531 152537 152539 152545 152549 152551 152555 152561 152567 152569 152575 152579 152581 152587 152591 152597 152605 203614
| A. | 酸碱中和滴定时,用待测液润洗锥形瓶. | |
| B. | 酸碱中和滴定时,用冲洗干净的滴定管盛装标准溶液 | |
| C. | 用NaOH标准溶液测定未知度的盐酸时,选用酚酞作指示剂,实验时不小心多加了几滴 | |
| D. | 用标准盐酸测定未知浓度NaOH结束实验,酸式滴定管尖嘴部分有气泡,开始实验时无气泡 |